BioTech
CRISPR наступного покоління підвищує точність генної терапії
Securities.io дотримується суворих редакційних стандартів і може отримувати винагороду за перевірені посилання. Ми не є зареєстрованим інвестиційним консультантом, і це не є інвестиційною порадою. Будь ласка, перегляньте наші розкриття партнерів.

Підвищення точності редагування генів
Донедавна генетичні модифікації були досить грубими, вставляючи нову генетичну послідовність випадковим чином у цільові організми.
Метод введення також був дуже руйнівним. Як наслідок, лише бактерії та рослини регулярно піддавалися генетичній модифікації, а будь-яке редагування генів у організмах, таких як ссавці (включаючи людей), було складним, дорогим і повільним.
Це частково змінилося завдяки технології CRISPR, яка раптово відкрила шлях для точного та контрольованого редагування генів, що призвело до схвалення першої генної терапії для лікування генетичних захворювань людини наприкінці 2023 року.
Однак CRISPR все ще не ідеальний, що іноді призводить до небажаних генетичних модифікацій.
Можливо, це щойно змінилося завдяки проривному відкриттю трьох дослідників Массачусетського технологічного інституту.
Вони оголосили про новий метод, який дозволяє радикально покращити надійність редагування генів, відкриваючи шлях для створення нових методів лікування.
Вони опублікували свої результати у престижному науковому журналі Nature1, під назвою «Розроблені основні редактори з мінімальними геномними помилками".
Від стандартного CRISPR до Prime Editing
З моменту схвалення перших методів лікування на основі CRISPR-Cas9, ідея надійного редагування геномів пацієнтів для їх лікування перестала бути науковою фантастикою. Однак технологія CRISPR не завжди модифікує цільовий ген так, як задумали вчені.
Система CRISPR складається з ферменту під назвою Cas9, який може розрізати дволанцюгову ДНК у певному місці, а також направляючої РНК, яка вказує Cas9, де розрізати.
Дослідники адаптували цей підхід для вирізання дефектних послідовностей генів або для вставки нових, дотримуючись шаблону РНК.
З 2019 року дослідники Массачусетського технологічного інституту опублікували нову концепцію під назвою «prime editing» (елементарне редагування), яка є точнішою, ніж звичайне редагування генів CRISPR-Cas9. Як результат, вона має менше побічних ефектів і меншу ймовірність спричинити додаткові проблеми зі здоров’ям у часто і без того ослаблених пацієнтів.
Прайм-редатинг використовує модифікований Cas9, злитий з ферментом зворотної транскриптази, що дозволяє йому виконувати всі можливі модифікації генетичних основ, а також невеликі вставки та делеції генетичних послідовностей.
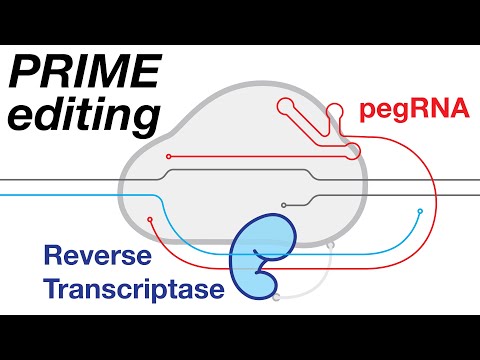
Тож у довгостроковій перспективі очікується, що первинне редагування стане вдосконаленою та надійнішою версією редагування генів на основі CRISPR.

джерело: Бенджамін Маклеод
Наприклад, у 2025 році основні редактори були успішно використані для лікування пацієнта з хронічною гранулематозною хворобою (ХГХ) – рідкісним генетичним захворюванням, яке вражає лейкоцити.
«В принципі, цю технологію зрештою можна буде використовувати для лікування сотень генетичних захворювань шляхом виправлення невеликих мутацій безпосередньо в клітинах і тканинах».
Але його потрібно було трохи вдосконалити, перш ніж він буде готовий до використання в клітинах та тілах людей.
Як Prime Editing покращує точність вставки ДНК
Первинне редагування розрізає лише один із комплементарних ланцюгів цільової послідовності ДНК, відкриваючи клапан, де можна вставити нову послідовність.
Однак, після копіювання нової послідовності, вона повинна конкурувати зі старим ланцюгом ДНК, щоб бути включеною в геном.
Якщо старий ланцюг перемагає новий, зайвий клапоть новоствореної ДНК, що звисає, може випадково потрапити кудись ще, що призведе до помилок.
Такі помилки можуть зрештою спричинити рак, випадково вбудовуючись у геном, і цей ризик необхідно зменшити.
У найновішій версії редакторів Prime цей рівень помилок коливається від однієї на сім редагувань до однієї на 121 редагування для різних режимів редагування, що все ще занадто високо.
«Технології, які ми маємо зараз, справді набагато кращі за попередні інструменти генної терапії, але завжди існує ризик цих непередбачуваних наслідків».
Значний стрибок у надійності Prime Editing
У 2023 році дослідники Массачусетського технологічного інституту виявили, що деякі мутовані версії білка Cas9, що використовуються в первинному редагуванні, іноді переміщуються на одну або дві основи далі вздовж послідовності ДНК, а не завжди в одному й тому ж місці.
Це зробило старі ланцюги ДНК менш стабільними, тому вони деградували, що полегшило включення нових ланцюгів без будь-яких помилок.
У цьому новому дослідженні 2025 року дослідники виявили кілька мутацій Cas9, які знизили рівень помилок до 1/20 від початкового значення.
При штучному поєднанні цих мутацій в одному білку Cas9 вони знизили рівень помилок до 1/36 від початкової кількості.
«У цій статті окреслено новий підхід до редагування генів, який не ускладнює систему доставки та не додає додаткових кроків, але призводить до набагато точнішого редагування з меншою кількістю небажаних мутацій».
Не задовольняючись цим, вони також використали систему первинного редагування, яка має РНК-зв'язуючий білок, що ефективніше стабілізує кінці РНК-матриці.
Фінальна версія їхнього набору інструментів для редагування генів, що отримала назву vPE, мала рівень помилок лише в 1/60 від оригіналу, або лише від 101 до 543 редагувань, залежно від використаних режимів редагування.
Проведіть пальцем, щоб прокрутити →
| Версія Prime Editor | Приблизний коефіцієнт помилок | Покращення проти оригіналу |
|---|---|---|
| Оригінальний головний редактор | 1 помилка на 7–121 редагування | Базова лінія |
| Мутовані варіанти Cas9 | Початковий коефіцієнт помилок 1/20–1/36 | До 36× точніше |
| vPE (стабілізований РНК) | 1/60 початкового коефіцієнта помилок | До 60× точніше |
Наступні кроки
Ще однією перешкодою редагування генів завжди була доставка білків для редагування генів та ДНК/РНК всередину ядра цільових клітин або ж вплив лише на певні тканини організму.
Тож це буде наступним фокусом дослідників, особливо враховуючи те, що методи первинного редагування обмежені поганою якістю виконання порівняно з меншими та простішими «традиційними» системами CRISPR-Cas9.
Вони також вважають, що цей інструмент має потенціал пришвидшити прогрес у біотехнологіях загалом, а не лише в методах редагування генів.
По-перше, методику та відкриття, що модифікація білка Cas9 може підвищити його надійність, можна було б застосувати до всіх технологій редагування генів на основі CRISPR, а не лише до первинного редагування.
По-друге, це може стати потужним поштовхом для інших дослідницьких проектів, що використовують редагування генів та геному як інструмент дослідження. Наприклад, пошук відповідей на питання про те, як розвиваються тканини, як еволюціонують популяції ракових клітин та як клітини реагують на медикаментозне лікування.
«Редактори геному широко використовуються в дослідницьких лабораторіях.»
Тож терапевтичний аспект захопливий, але ми справді раді бачити, як люди почнуть інтегрувати наших редакторів у свої дослідницькі процеси».
Зрештою, мутації, що покращують надійність Cas9, можливо, не всі були виявлені в цьому дослідженні. Тому подальший аналіз та оптимізація цієї нової концепції можуть дати ще кращі результати в майбутньому.
Інвестування в редагування генів
Illumina
(ILMN )
У той час як інші -оміки в мультиоміці (протеоміка, транскриптоміка тощо) важливі, майже всі так чи інакше пов'язані з геномікою, основним «інструкцієм з експлуатації» кожної живої клітини.
І, безумовно, найбільшим виробником машин для секвенування геному є Illumina. Компанія спеціалізується на зчитуванні коротких генетичних послідовностей, які використовуються для виявлення раку. Наразі вона має понад 22,000 165 встановлених секвенаторів у XNUMX країнах.
Близько половини витратних матеріалів для секвенаторів Illumina використовується в клінічних застосуваннях, а інша половина — у державних та приватних дослідницьких лабораторіях. У клінічних застосуваннях половина попиту припадає на онкологію.

джерело: Illumina
Оскільки геноміка та мультиоміка стають центром процесу розробки ліків, а також діагностики раку, очікується, що обладнання Illumina буде користуватися великим попитом.
Компанія очікує, що попит на NGS (секвенування наступного покоління) зросте на 18% у середньому на 6% для клінічного застосування та на 100% для досліджень, що збільшить загальний адресний ринок (TAM) сектору зі 25 мільярдів доларів для клінічного застосування до 2033 мільярдів доларів для досліджень до XNUMX року.

джерело: Illumina
У Illumina була складна історія з компанією Grail, що займається рідкою біопсією (ГРАЛЬ -0.36%), яка була відокремленою компанією Illumina, пізніше знову придбаною, а тепер змушеною знову виділитися антимонопольними органами США та ЄС.
Після вирішення цієї проблеми Illumina може відновити своє довгострокове зростання та зростання ціни акцій, особливо враховуючи, що зрештою тести рідкої біопсії Grail, ймовірно, все ще залежатимуть від секвенаторів Illumina.
Тим часом, збільшення кількості генних терапій також призведе до збільшення використання секвенаторів Illumina як у дослідженнях, так і в клінічних умовах.
(Ви також можете прочитати більш детальний аналіз бізнесу, майбутніх технологій та історії Illumina у спеціальному інвестиційному звіті.)
Останні новини та розробки акцій Illumina (ILMN)
Посилання на дослідження
1. Чаухан, В.П., Шарп, П.А. та Лангер, Р. Розроблені основні редактори з мінімальними геномними помилками. Nature (2025). https://doi.org/10.1038/s41586-025-09537-3











