BioTech
CRISPR der nächsten Generation steigert die Genauigkeit in der Gentherapie
Securities.io hält strenge redaktionelle Standards ein und erhält möglicherweise eine Vergütung für geprüfte Links. Wir sind kein registrierter Anlageberater und dies stellt keine Anlageberatung dar. Bitte beachten Sie unsere Affiliate-Offenlegung.

Präzisere Genbearbeitung
Bis vor Kurzem waren genetische Modifikationen eher grobe Eingriffe, bei denen eine neue genetische Sequenz zufällig in die Zielorganismen eingefügt wurde.
Die Methode des Einfügens war zudem sehr destruktiv. Daher wurden routinemäßig nur Bakterien und Pflanzen genetisch verändert, während die Genombearbeitung bei Organismen wie Säugetieren (einschließlich des Menschen) komplex, teuer und langsam war.
Dies hat sich teilweise mit der CRISPR-Technologie geändert, die plötzlich den Weg für eine präzise und kontrollierte Genombearbeitung eröffnete. Dies führte dazu, dass Ende 2023 die erste Gentherapie für eine genetisch bedingte Erkrankung des Menschen zugelassen wurde..
Allerdings ist CRISPR noch nicht perfekt und führt manchmal zu unerwünschten genetischen Veränderungen.
Dies könnte sich durch eine bahnbrechende Entdeckung von drei MIT-Forschern gerade geändert haben.
Sie kündigten eine neue Methode an, die eine radikal verbesserte Zuverlässigkeit der Genombearbeitung ermöglicht und den Weg für die Entwicklung neuer Therapien ebnet.
Sie veröffentlichten ihre Ergebnisse in der renommierten wissenschaftlichen Zeitschrift Nature1, unter dem Titel "Entwickelte Prime-Editoren mit minimalen genomischen Fehlern".
Von Standard-CRISPR bis Prime Editing
Seit der Zulassung der ersten CRISPR-Cas9-basierten Therapien ist die Idee, das Genom von Patienten zuverlässig zu verändern und so zu heilen, keine Science-Fiction mehr. Allerdings verändert die CRISPR-Technologie das Zielgen nicht immer so, wie es die Wissenschaftler beabsichtigen.
Das CRISPR-System besteht aus einem Enzym namens Cas9, das doppelsträngige DNA an einer bestimmten Stelle schneiden kann, sowie einer Leit-RNA, die Cas9 mitteilt, wo es schneiden soll.
Forscher haben diesen Ansatz angepasst, um fehlerhafte Gensequenzen herauszuschneiden oder neue einzufügen, wobei sie einer RNA-Vorlage folgten.
Seit 2019 veröffentlichen MIT-Forscher ein neues Konzept namens Prime Editing, das präziser ist als die herkömmliche CRISPR-Cas9-Genbearbeitung. Dadurch treten weniger unerwünschte Effekte auf und es besteht ein geringeres Risiko, bei oft bereits geschwächten Patienten zusätzliche gesundheitliche Probleme zu verursachen.
Beim Prime Editing wird ein modifiziertes Cas9 verwendet, das mit einem Reverse-Transkriptase-Enzym fusioniert ist, wodurch alle möglichen genetischen Basenmodifikationen sowie kleine Einfügungen und Löschungen genetischer Sequenzen durchgeführt werden können.
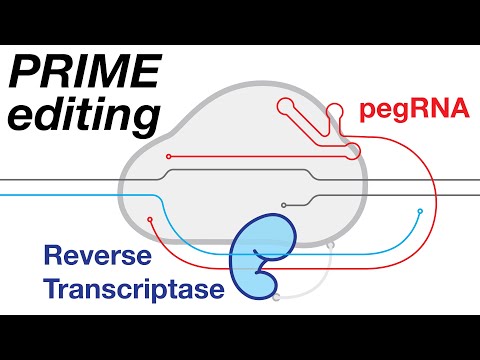
Daher ist zu erwarten, dass sich Prime Editing langfristig zur verbesserten und zuverlässigeren Version der CRISPR-basierten Genombearbeitung entwickelt.

Quelle: Benjamin McLeod
So wurden beispielsweise im Jahr 2025 Prime-Editoren erfolgreich zur Behandlung eines Patienten mit chronischer Granulomatose (CGD) eingesetzt, einer seltenen genetischen Erkrankung, die die weißen Blutkörperchen betrifft.
„Grundsätzlich könnte diese Technologie letztendlich dazu eingesetzt werden, viele Hunderte genetischer Erkrankungen zu behandeln, indem kleine Mutationen direkt in Zellen und Geweben korrigiert werden.“
Vikash Chauhan - Koch-Institut für Integrative Krebsforschung des MIT
Es musste jedoch noch etwas verbessert werden, bevor es für den Einsatz in menschlichen Zellen und Körpern bereit war.
Wie Prime Editing die Genauigkeit der DNA-Insertion verbessert
Beim Prime Editing wird nur einer der komplementären Stränge der Ziel-DNA-Sequenz geschnitten, wodurch eine Klappe geöffnet wird, in die eine neue Sequenz eingefügt werden kann.
Sobald die neue Sequenz kopiert wurde, muss sie jedoch mit dem alten DNA-Strang um die Aufnahme in das Genom konkurrieren.
Wenn der alte Strang den neuen verdrängt, kann es passieren, dass der zusätzliche Lappen neu entstandener DNA, der darüber hängt, versehentlich an einer anderen Stelle eingebaut wird, was zu Fehlern führt.
Solche Fehler könnten letztlich Krebs verursachen, indem sie sich zufällig in das Genom einfügen. Dies stellt ein klares Risiko dar, das verringert werden muss.
Bei der aktuellsten Version der Prime-Editoren liegt diese Fehlerrate bei verschiedenen Bearbeitungsmodi zwischen einer pro sieben Bearbeitungen und einer pro 121 Bearbeitungen, was immer noch zu hoch ist.
„Die Technologien, die wir heute haben, sind wirklich viel besser als frühere Gentherapie-Tools, aber es besteht immer die Möglichkeit dieser unbeabsichtigten Folgen.“
Vikash Chauhan - Koch-Institut für Integrative Krebsforschung des MIT
Großer Sprung in der Zuverlässigkeit der Prime-Bearbeitung
Im Jahr 2023 entdeckten die MIT-Forscher, dass einige mutierte Versionen des bei der Prime Editing verwendeten Cas9-Proteins ihren Schnitt manchmal ein oder zwei Basen weiter entlang der DNA-Sequenz vornahmen, anstatt immer an derselben Stelle.
Dadurch wurden die alten DNA-Stränge weniger stabil und zersetzten sich, was den fehlerfreien Einbau der neuen Stränge erleichterte.
In dieser neuen Studie aus dem Jahr 2025 haben die Forscher mehrere Cas9-Mutationen identifiziert, die die Fehlerrate auf 1/20 ihres ursprünglichen Werts gesenkt haben.
Durch die künstliche Kombination dieser Mutationen in einem einzigen Cas9-Protein sank die Fehlerrate auf 1/36 des ursprünglichen Wertes.
„Dieses Papier skizziert einen neuen Ansatz zur Genomeditierung, der das Abgabesystem nicht komplizierter macht und keine zusätzlichen Schritte erfordert, aber zu einer viel präziseren Bearbeitung mit weniger unerwünschten Mutationen führt.“
Philipp Scharf - Koch-Institut für Integrative Krebsforschung des MIT
Damit nicht genug, verwendeten sie zusätzlich ein Prime-Editing-System mit einem RNA-bindenden Protein, das die Enden der RNA-Vorlage effizienter stabilisiert.
Die endgültige Version ihres Toolkits zur Genbearbeitung, genannt vPE, hatte eine Fehlerrate von nur 1/60 der ursprünglichen Version oder nur 101–543 Bearbeitungen, je nach den verwendeten Bearbeitungsmodi.
Zum Scrollen wischen →
| Prime Editor Version | Ungefähre Fehlerrate | Verbesserung vs. Original |
|---|---|---|
| Ursprünglicher Prime-Editor | 1 Fehler pro 7–121 Bearbeitungen | Baseline |
| Mutierte Cas9-Varianten | 1/20–1/36 ursprüngliche Fehlerrate | Bis zu 36x präziser |
| vPE (RNA-stabilisiert) | 1/60 ursprüngliche Fehlerrate | Bis zu 60x präziser |
Die nächsten Schritte
Eine weitere Hürde bei der Genomeditierung bestand schon immer darin, die Genomeditierungsproteine und DNA/RNA in den Zellkern der Zielzellen zu bringen oder nur bestimmte Gewebe im Körper anzuvisieren.
Dies wird der nächste Schwerpunkt der Forscher sein, insbesondere da die Leistungsfähigkeit der Prime-Editing-Techniken im Vergleich zu kleineren und einfacheren „traditionellen“ CRISPR-Cas9-Systemen eingeschränkt ist.
Sie sind außerdem der Meinung, dass dieses Tool das Potenzial hat, den Fortschritt in der Biotechnologie insgesamt zu beschleunigen, nicht nur bei Therapien zur Genomeditierung.
Erstens könnten die Technik und die Entdeckung, dass die Modifikation des Cas9-Proteins dessen Zuverlässigkeit verbessern kann, auf alle CRISPR-basierten Technologien zur Genomeditierung angewendet werden, nicht nur auf die Primärbearbeitung.
Zweitens könnte dies anderen Forschungsprojekten, die die Gen- und Genomeditierung als Forschungsinstrument nutzen, einen enormen Schub verleihen. So könnten beispielsweise Antworten auf die Frage gefunden werden, wie sich Gewebe entwickelt, wie sich Krebszellpopulationen entwickeln und wie Zellen auf eine medikamentöse Behandlung reagieren.
„Genom-Editoren werden in Forschungslabors umfassend eingesetzt.
Der therapeutische Aspekt ist also spannend, aber wir sind wirklich gespannt, wie die Leute beginnen, unsere Editoren in ihre Forschungsabläufe zu integrieren.“
Vikash Chauhan - Koch-Institut für Integrative Krebsforschung des MIT
Schließlich wurden möglicherweise nicht alle Mutationen, die die Cas9-Zuverlässigkeit verbessern, in dieser Studie gefunden. Daher könnten weitere Analysen und Optimierungen dieses neuen Konzepts in Zukunft zu noch besseren Ergebnissen führen.
Investitionen in die Genom-Editierung
Illumina
(ILMN )
Während die andere -omik in der Multiomik (Proteomik, Transkriptomik usw.) wichtig sind, drehen sich fast alle auf die eine oder andere Weise um die Genomik, die zentrale „Bedienungsanleitung“ jeder lebenden Zelle.
Der mit Abstand größte Hersteller von Genomsequenzierungsgeräten ist Illumina. Das Unternehmen konzentriert sich auf die Analyse kurzer Gensequenzen, die zur Krebserkennung eingesetzt werden. Derzeit sind über 22,000 Sequenzer in 165 Ländern installiert.
Etwa die Hälfte der Verbrauchsmaterialien der Sequenziergeräte von Illumina wird in klinischen Anwendungen eingesetzt, die andere Hälfte in öffentlichen und privaten Forschungslabors. Bei klinischen Anwendungen kommt die Hälfte der Nachfrage aus der Onkologie.

Quelle: Illumina
Da Genomik und Multiomik in den Mittelpunkt der Arzneimittelforschung sowie der Krebsdiagnostik rücken, ist mit einer hohen Nachfrage nach den Geräten von Illumina zu rechnen.
Das Unternehmen erwartet, dass die Nachfrage nach NGS (Next Generation Sequencing) bei klinischen Anwendungen um durchschnittlich 18 % und bei der Forschung um durchschnittlich 6 % jährlich steigen wird. Dadurch wird der gesamte adressierbare Markt (TAM) des Sektors bis 100 von 25 Milliarden US-Dollar für klinische Anwendungen auf 2033 Milliarden US-Dollar für die Forschung anwachsen.

Quelle: Illumina
Illumina hatte eine komplizierte Geschichte mit dem Flüssigbiopsie-Unternehmen Grail (GRAL -0.36 %), das ein Spin-off von Illumina war, später zurückgekauft wurde und nun von den Wettbewerbsbehörden in den USA und der EU erneut zu einem Spin-off gezwungen wurde.
Wenn dieses Problem aus dem Weg geräumt ist, könnte Illumina sein langfristiges Wachstum und den Anstieg seines Aktienkurses wieder aufnehmen, insbesondere da die Flüssigbiopsietests von Grail letztlich wahrscheinlich weiterhin auf Sequenzern von Illumina basieren werden.
Gleichzeitig wird durch die zunehmende Zahl von Gentherapien auch die Verwendung der Sequenzer von Illumina sowohl in der Forschung als auch im klinischen Umfeld zunehmen.
(Lesen Sie auch Eine detailliertere Analyse des Geschäfts, der zukünftigen Technologien und der Geschichte von Illumina finden Sie im speziellen Investitionsbericht.)
Aktuelle Illumina (ILMN) Aktiennachrichten und -entwicklung
Zitierte Studie
1. Chauhan, VP, Sharp, PA & Langer, R. Entwickelte Prime-Editoren mit minimalen genomischen Fehlern. Natur (2025). https://doi.org/10.1038/s41586-025-09537-3











