Biotechnologies
Yale dévoile une avancée majeure basée sur Cas12a pour l'édition CRISPR multigénique
Securities.io applique des normes éditoriales rigoureuses et peut percevoir une rémunération pour les liens vérifiés. Nous ne sommes pas un conseiller en investissement agréé et ceci ne constitue pas un conseil en investissement. Veuillez consulter notre divulgation de l'affiliation.

Développer le potentiel de CRISPR
Depuis sa découverte, CRISPR (« Clustered Regularly Interspaced Short Palindromic Repeats »), qui a remporté le Prix Nobel de Chimie 2020, a révolutionné la médecine et la biotechnologie.

Source: Prix Nobel
C'est parce que CRISPR est la première méthode d'édition génétique qui permet un ciblage très précis d'une séquence génétique spécifique, permettant de corriger les erreurs génétiques soit in vitro or in vivo sans risquer de mutations indésirables.
Ceci est important car l’insertion non dirigée de gènes a été liée à des problèmes majeurs, notamment des risques de cancer, ce qui rend leur utilisation thérapeutique difficile et controversée.
CRISPR peut être utilisé de plusieurs façons pour interrompre un gène déjà présent, supprimer une séquence spécifique ou modifier/insérer la bonne séquence génétique.

Source: Thérapeutique CRISPR
Cela s'est transformé en une avancée médicale avec la Approbation de la FDA pour le premier basé sur CRISPR thérapie en 2023, développé par Thérapeutique CRISPR pour les maladies génétiques du sang (suivez le lien pour un rapport dédié à CRISPR Therapeutics).
Cependant, les thérapies CRISPR et le génie génétique ne peuvent modifier qu’un seul gène à la fois et peuvent être difficiles à concevoir.
Il se pourrait donc qu’une nouvelle ère s’ouvre pour la technologie CRISPR, grâce au travail des chercheurs de l’Université de Yale, qui ont développé une nouvelle méthode CRISPR capable de modifier plusieurs gènes à la fois.
Il s’agit d’une étude révolutionnaire qui a réuni une équipe massive de chercheurs : pas moins de 37 personnes sont mentionnées comme auteurs de l’étude1 publié dans Nature Biomedical Engineering sous le titre «Souris knock-in Cas12a pour l'édition multiplexée du génome, la modélisation des maladies et l'ingénierie des cellules immunitaires ».
Cela pourrait aider à générer de nouveaux modèles de maladies et de traitements, tels que les maladies génétiques du foie, le cancer du poumon et le cancer de la peau, et accélérer les recherches dans ce domaine.
Les nombreux systèmes CRISPR
Lorsque l’on parle de CRISPR, que ce soit dans le cadre de sa découverte initiale récompensée par le prix Nobel ou dans le cadre des thérapies déjà approuvées par la FDA, c’est en fait de CRISPR-Cas9 dont on parle.
La protéine « Cas » du système est la protéine responsable de la coupure du brin d'ADN et de l'édition génique, guidée par un brin d'ARN. De nombreuses autres protéines Cas sont actuellement étudiées, et d'autres encore restent probablement à découvrir.
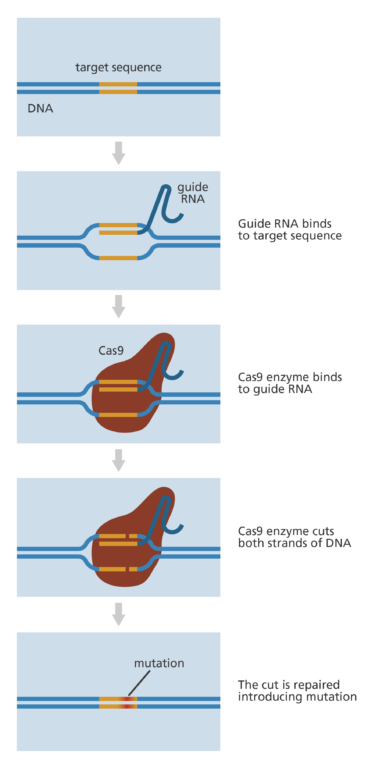
Source: Votre Génome
Il pourrait même, à long terme, devenir courant pour les chercheurs de simplement concevoir des systèmes Cas personnalisés, notamment avec « OpenCRISPR-1 », une IA open source conçue pour concevoir un système CRISPR personnalisé pour des situations spécifiquesUne simulation informatique appelée CREME (Explications du modèle d'éléments de régulation cis) pourrait également aider à mieux comprendre comment optimiser les systèmes CRISPR.
Parmi ces multiples systèmes CRISPR au-delà de CRISPR-Cas9, aucun n’a été aussi étudié et n’est aussi proche d’une application pratique que CAs12a.
CRISPR-Cas12a
Depuis que nous en avons discuté pour la première fois en 2023, de nombreux progrès ont été réalisés sur la technologie Cas12a.
CRISPR-Cas12a est un système différent de Cas9 sur plusieurs aspects :
- Fournit des sites de coupe alternatifs à ce que Cas9 peut faire.
- les problèmes difficiles à résoudre avec Cas9 pourraient être résolus avec Cas12.
- Il coupe l’ADN d’une manière qui laisse une section « collante » d’ADN au lieu de la coupe « émoussée » de Cas9 et peut être coupé plusieurs fois.
-
- Cela augmente les risques d’édition génétique.
- Il n'y a pas besoin d'un ARNc transactivant (tracrRNA)pour Cas12a, contrairement à Cas9. En raison de sa taille réduite, il permettrait une édition multiplex du génome plus facile.
- Plus d'un gène peut être modifié à la fois avec CAs12a.

Source: Wikipédia
C'est cette dernière caractéristique de Cas12a qui a suscité le plus d'intérêt chez les biologistes, car de nombreuses maladies ou le génie génétique nécessitent de multiples modifications, insertions et/ou suppressions de gènes.
Ainsi, même s’il est théoriquement possible (bien que coûteux) d’effectuer une série d’éditions de gènes CRISPR-Cas9 lors de la création, par exemple, d’une nouvelle variété de maïs, ce n’est pas une option viable pour les maladies multigéniques.
Entre-temps, il devient évident que le potentiel de CRISPR va bien au-delà de la guérison des maladies génétiques rares : la neurologie, le cancer (oncologie) et les problèmes métaboliques sont les plus susceptibles d’améliorer ou de sauver la vie de dizaines de millions de personnes.

Source: ARK Investir
Le problème est que pour la plupart des thérapies liées aux maladies non génétiques, la gestion de multiples modifications génétiques in vivo sera une exigence absolue.
Étude Cas12a de Yale
Cibles diverses
Avant de procéder à une édition multigénique sur des humains, nous devons d’abord mieux comprendre l’effet d’une intervention aussi agressive sur le génome.
Les chercheurs de Yale ont utilisé des souris de laboratoire pour modifier génétiquement des cellules immunitaires, notamment des lymphocytes T CD4+ et CD8+, des lymphocytes B et des cellules dendritiques dérivées de la moelle osseuse. Ils ont également modifié des gènes liés au cancer et des tissus hépatiques in vivo.
Le matériel d'édition de gènes CRISPR a été délivré à chaque cible avec des rétrovirus, des virus adéno-associés et des nanoparticules lipidiques, respectivement.
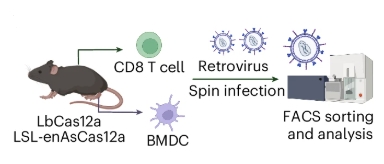
Source: Nature Biomedical Engineering
Afin d’élargir les possibilités de la méthode, ils ont également utilisé 2 variantes de Cas12a.
Vérification de l'efficacité
Dans un premier temps, les chercheurs ont associé la mutation à une protéine fluorescente pour vérifier si elle se déroulait correctement.
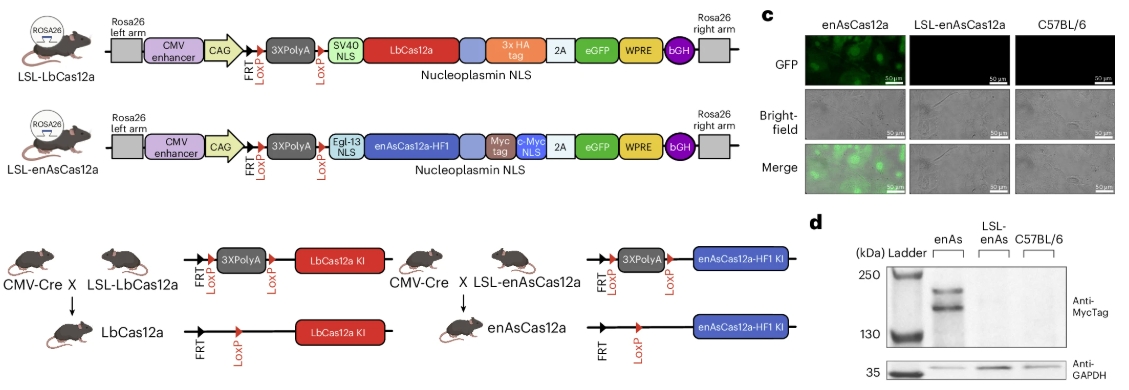
Source: Nature Biomedical Engineering
Ils ont ensuite vérifié comment l'efficacité de l'édition génétique variait selon les organes ciblés. Il est apparu que le foie, le cerveau, les reins et les poumons étaient parmi les organes les plus faciles à optimiser pour l'édition génétique in vivo.
Cela donne des résultats très prometteurs, car ces organes sont les plus importants pour les cibles médicales clés des futures thérapies CRISPR.

Source: Nature Biomedical Engineering
Potentiel pratique
Une fois le potentiel du concept prouvé, les chercheurs ont ensuite testé des cas d’utilisation consistant à modifier les cellules immunitaires et les cellules cancéreuses.
En ce qui concerne les cellules immunitaires, l’efficacité de la transformation, la mesure mesurant la quantité totale de cellules exposées qui sont génétiquement modifiées, était remarquablement élevée, atteignant jusqu’à 90-100 %.

Source: Nature Biomedical Engineering
Un autre résultat remarquable, indispensable à toute application potentielle des thérapies in vivo, est un taux très élevé de mutations ciblées. Cela signifie que seul le gène visé est modifié, et que très peu d'éditions de gènes hors cible se produisent.

Source: Nature Biomedical Engineering
DAKO
Poussant encore plus loin la possibilité de la technologie CIRSPR-Cas12a, les chercheurs ont développé une nouvelle activation et élimination à double gène (DAKO).
Cela signifie qu'un seul traitement peut ultérieurement se diviser et produire à la fois l'activation d'un gène et la suppression d'un autre.
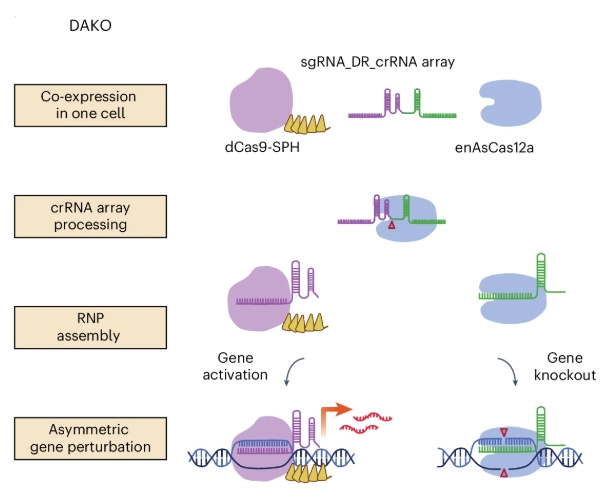
Source: Nature Biomedical Engineering
Il s'agit d'une étape importante pour modifier des cellules dotées de mécanismes biochimiques complexes, par exemple lorsqu'une protéine active un mécanisme et qu'une autre le supprime. L'édition génique DAKO permet à la fois d'augmenter l'activité souhaitée au-delà des niveaux normaux et d'éliminer le système qui inhiberait cet effet.
Les rétrocontrôles indésirables ou mal gérés étant souvent une raison clé pour laquelle l'édition génétique ne fonctionne pas comme espéré, ce système DAKO pourrait s'avérer être une révolution, notamment en oncologie, en neurologie et dans les traitements métaboliques.
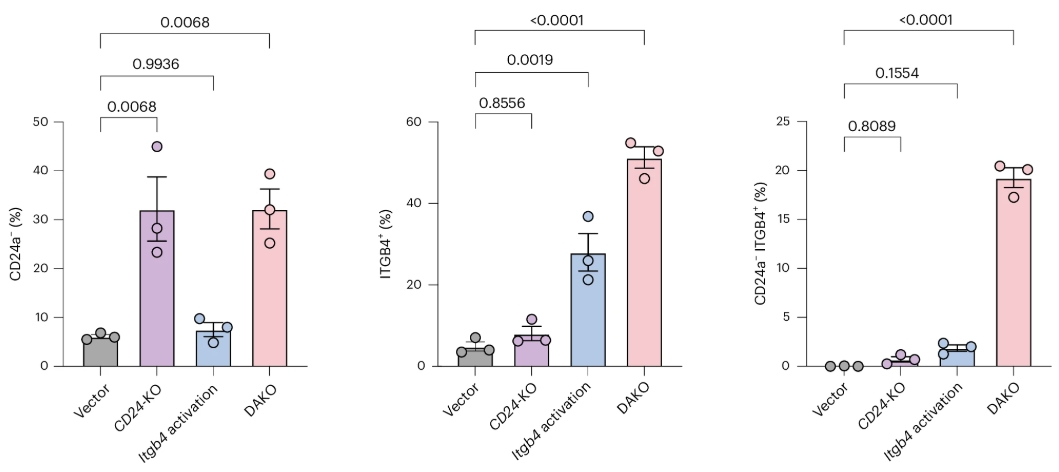
Source: Nature Biomedical Engineering
Modèles animaux
Ce nouveau système d'édition génétique utilisant Cas12a peut être aussi précis que Cas9 mais peut effectuer plusieurs modifications à la fois, et ces modifications peuvent être à la fois l'activation et la suppression de gènes.
Cela en fait un système parfait pour créer un nouveau modèle biologique sur lequel les biologistes peuvent tester leurs hypothèses.
Ces modèles animaux sont essentiels pour tester des traitements potentiels ou mieux comprendre des maladies complexes. Ainsi, même si aucune thérapie utilisant Cas12a n'est jamais commercialisée, ce seul fait signifierait que cette variante de CRISPR aurait un impact considérable sur la recherche biotechnologique future.
Aller plus loin
Comme il a été prouvé dans l’étude que l’intensité de l’édition génétique peut varier considérablement selon l’organe, il est probable que d’autres améliorations puissent être obtenues.
Un élément clé consistera probablement à tester de nouveaux vecteurs pour le système d'édition génétique, qu'il s'agisse d'autres virus ou d'autres nanocapsules lipidiques. En particulier, de meilleurs vecteurs pour les organes les moins affectés seront nécessaires pour des études ou des maladies spécifiques.
À long terme, il est très probable que les thérapies d’édition génétique pour les maladies complexes comme le cancer et les problèmes neurologiques utiliseront un système plus proche de ce système cas12a que du système monogénique « traditionnel » Cas9.
Société Cas12a
Modifier
(EDIT )
Editas a été fondée par Jennifer Doudna, co-découvreuse de CRISPR-Cas9. Editas a commencé à travailler avec Cas9, mais se concentre désormais sur une version propriétaire de Cas12a qu'elle a conçue : AsCas12a.
Vous pouvez en savoir plus sur les propriétés uniques de Cas12a dans notre article dédié «Qu’est-ce que CRISPR-Cas12a2 ? & En quoi est-ce important? ».

Source: Modifier
Vous pouvez également lire un aperçu de toutes les entreprises de Jennifer Doudna dans l'article correspondant «Principales entreprises de Jennifer Doudna à surveiller. »
Editas se concentre sur la drépanocytose (SCD) et la bêta-thalassémie, 2 maladies pour lesquelles il a perdu la course à l'approbation du premier traitement face à ses concurrents CRISPR Therapeutics et BlueBirdBio.
Dans l'ensemble, le programme SCD (récemment renommé reni-cell) a été retardé à plusieurs reprises, suscitant l'inquiétude des investisseurs, et a depuis été recentré sur la thérapie in vivo pour la distinguer des thérapies SCD déjà approuvées.
Néanmoins, Editas possède des brevets importants sur CRISPR-Cas12, qui a été utilisé par des chercheurs de l'Université de Nouvelle-Galles du Sud, en Australie, développer un test de bandelettes COVID-19, illustrant le potentiel technologique au-delà de l’édition génétique.
Editas se concentre sur d’autres versions de CRISPR que le « classique » CRISPR-Cas9 et sa propriété intellectuelle de recherche pourrait s’avérer utile pour établir des partenariats et générer des revenus sans produit approuvé par la FDA, en plus d’une fuite de liquidités jusqu’en 2026.
Alors que Cas12a semble de plus en plus s'avérer être la meilleure méthode de sa catégorie pour l'édition multigénique, l'expertise d'Editas et la concentration de son pipeline sur cette variante CRISPR pourraient s'avérer un pari gagnant à long terme.
(Vous pouvez en savoir plus sur CRISPR compandans notre article correspondant «Top 5 des entreprises CRISPR dans lesquelles investir ».)
Dernières nouvelles sur Editas
Études référencées :
1. Tang, K., Zhou, L., Tian, X. et al. Souris knock-in Cas12a pour l'édition multiplexée du génome, la modélisation des maladies et l'ingénierie des cellules immunitaires. Nat. Biomédical. Eng (2025). https://doi.org/10.1038/s41551-025-01371-2











