BioTech
DNA-Roboter erklärt: Die Zukunft von Medizin und Informatik

Robotereinführung schreitet rasch vorangetrieben durch sinkende Kosten, steigende Nachfrage und die Integration künstlicher Intelligenz (KI).
Nach Angaben der US-Organisation Statistiken zur Weltrobotik 2025 Bei Industrierobotern wurden im Jahr 2024 542,000 Roboter installiert. Dies markierte die „zweithöchste jährliche Installationszahl von Industrierobotern in der Geschichte – nur 2 % niedriger als der Rekordwert vor zwei Jahren“, sagte Takayuki Ito, Präsident der International Federation of Robotics.
Neben Fabrikhallen werden Roboter auch aktiv auf Flughäfen, in der Landwirtschaft, in Büros, beim Militär und im Weltraum eingesetzt, da sie sich von starren, vorprogrammierten Maschinen zu adaptiven, intelligenten Systemen weiterentwickeln.
Roboter sind nicht mehr nur mechanische Arme; dank Fortschritten in der Materialwissenschaft, der Miniaturisierung und der künstlichen Intelligenz werden sie vielmehr intelligenter, kleiner und vielseitiger.
Dies hat zu einem tiefgreifenden Wandel in der Medizin geführt: Operationsroboter ermöglichen minimalinvasive Eingriffe mit einer bisher unerreichten Präzision. Mikrorobotik und biobasierte Systeme versprechen gezielte Therapien, die Nebenwirkungen deutlich reduzieren können.
Selbst die Vorstellung von Maschinen, die im menschlichen Körper operieren, wird immer mehr zur wissenschaftlichen Realität.
Eintritt ins Zeitalter der molekularen Robotik
Ein neues Forschungsfeld in der Robotik ist eine aufkommende Klasse von mikroskopische Maschinen Aus DNA hergestellt und für den Betrieb im menschlichen Körper konzipiert.
Das Konzept der DNA-Nanotechnologie wurde vor einigen Jahrzehnten von Professor Nadrian Seeman, der weithin als Begründer dieses Forschungsgebiets gilt, erstmals vorgestellt. In den Anfangsjahren verlief der Fortschritt jedoch aufgrund hoher Kosten und der noch nicht ausgereiften DNA-Synthesetechnologien schleppend.
Fortschritte bei der chemischen DNA-Synthese zu Beginn des 21. Jahrhunderts senkten die Produktionskosten drastisch und beschleunigten die Entwicklung der DNA-Nanotechnologie.
Ein bedeutender Durchbruch gelang tatsächlich vor zwei Jahrzehnten, als Paul Rothemund die DNA-Origami-Technik einführte, die die Herstellung von Nanostrukturen durch die Bottom-up-Selbstorganisation der DNA ermöglichte und sich seither zu einer der am weitesten verbreiteten Strategien für den Bau von DNA-Robotern entwickelt hat.

Diese winzigen Geräte bestehen aus biologischen Molekülen, die sich im Körper bewegen, mit Zellen interagieren und hochspezifische Aufgaben ausführen können. Da diese Systeme aus demselben Grundmaterial bestehen, das auch den Körper durchzieht, können sie – anders als herkömmliche Roboter – nahtlos in biologischen Umgebungen funktionieren.
Eine neue Studie veröffentlicht in der Fachzeitschrift SmartBot1 verdeutlicht, wie weit dieses Fachgebiet gekommen ist. Es veranschaulicht die Entwicklung von DNA-Maschinen von frühen Ideen hin zu komplexeren, praktischeren und leistungsfähigeren Systemen, die eines Tages Medikamente direkt an erkrankte Zellen abgeben oder sogar Viren im Körper identifizieren und neutralisieren könnten.
Ihr Potenzial reicht noch viel weiter und umfasst die Einzelmolekülanalyse, die Nanofabrikation auf atomarer Ebene und sogar den Bau extrem kleiner Computergeräte und Datenspeichersysteme.
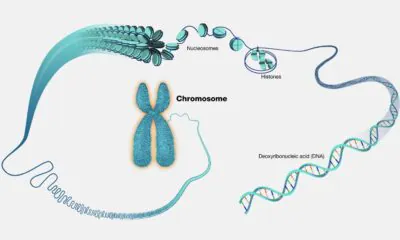
In ihrer detaillierten Studie erklären Forscher der Peking-Universität (PKU), wie DNA zur Herstellung funktionaler Maschinen genutzt wird. Dieselbe DNA, Desoxyribonukleinsäure, die in nahezu allen Lebewesen die genetische Information trägt, wird hier verwendet. Sie ist ein ideales und vielseitiges Baumaterial für den Bau mikroskopischer Roboter mit komplexen Geometrien, präzise definierten Abmessungen und multifunktionalen Fähigkeiten.
Das liegt an der einfachen Synthese der DNA, ihrer Fähigkeit zur präzisen Selbstorganisation, ihrer strukturellen Stabilität und ihrer Programmierbarkeit. Das Molekül bietet einen besonders einzigartigen Vorteil hinsichtlich seiner „mechanischen Programmierbarkeit“, wie die Studie feststellte. Während Einzelstränge (ssDNA) Flexibilität gewährleisten, verleihen doppelsträngige Abschnitte (dsDNA) den Designs Struktur, und zusammen ergeben sie ein klares Design-Werkzeugset.
Aufgrund dieser Eigenschaften sowie der Fortschritte in der strukturellen DNA-Nanotechnologie haben sich DNA-Roboter, die oft auch als DNA-Nanomaschinen oder Nanoroboter bezeichnet werden, rasant weiterentwickelt.
Um diese winzigen Roboter zu entwickeln, kombinieren Wissenschaftler traditionelle Robotik mit DNA-Faltungstechniken, wodurch Bewegung und zuverlässige Aufgabenerfüllung mit hoher Genauigkeit ermöglicht werden.
DNA-Roboter befinden sich zwar noch in der Entwicklungsphase und stehen vor erheblichen Herausforderungen. Trotz dieser Schwierigkeiten schreitet das Forschungsgebiet voran, da Wissenschaftler lernen, DNA-Strukturen zu entwerfen, die sich biegen, greifen, falten und auf Befehl bewegen können.
Damit unterstreicht die Arbeit eine Zukunft, in der diese programmierbaren biologischen Maschinen als Präzisionsinstrumente für Diagnose, Behandlung und Krankheitsprävention dienen können und möglicherweise die Medizin im Kern verändern.
„Die Roboter von morgen werden nicht nur aus Metall und Kunststoff bestehen“, stellte das Forschungsteam fest. „Sie werden biologisch, programmierbar und intelligent sein. Sie werden die Werkzeuge sein, die es uns ermöglichen, die molekulare Welt endlich zu beherrschen.“
Die Herausforderung der Molekularbewegung meistern
Um molekulare Maschinen zu bauen, erforschen Wissenschaftler schon seit langer Zeit die DNA und untersuchen, wie sie zu funktionierenden Maschinen konstruiert werden kann.
Die frühen DNA-Bauteile waren sehr einfach konstruiert; sie konnten sich öffnen und schließen oder entlang einer vorgegebenen Bahn bewegen. Obwohl sie einfach waren, bewiesen sie, dass Bewegung auf molekularer Ebene möglich war.
Inzwischen gehen Wissenschaftler mit kreativen Designansätzen noch einen Schritt weiter. Dazu gehören die Integration flexibler Komponenten, der Aufbau fester DNA-Verbindungen für mehr Stabilität und die Verwendung von Origami-inspirierten Faltmethoden.
Beim DNA-Origami werden lange Stränge zu komplexen Formen gefaltet. Forscher verwenden Hunderte kleinerer Stränge, um einen einzelnen Strang in detaillierte Formen wie Kästen, Käfige und Zahnräder zu lenken. Während manche Konstruktionen Tausende von Komponenten enthalten können, fungieren andere als winzige Schalter, Laufroboter oder Greifer.
Forscher wenden also Prinzipien der traditionellen Großrobotik auf die Nanoskala an und ermöglichen so DNA-basierten Systemen, wiederholbare, kontrollierte Aufgaben auszuführen.
Doch um DNA in Maschinen zu verwandeln, bedarf es nicht nur einer Struktur, sondern auch einer Bewegung, und die extrem geringe Größe dieser DNA-Roboter stellt eine große Herausforderung für die Steuerung ihrer Bewegung in der chaotischen, sich ständig verändernden molekularen Umgebung dar.
| Schlüsselbereich | Momentane Situation | Systemfokus | Warum es wichtig ist |
|---|---|---|---|
| Kernmaterial | Konventionelle Roboter basieren auf Metallen, Chips und Motoren. | DNA als programmierbares Baumaterial nutzen. | Ermöglicht es Maschinen, in biologischen Umgebungen zu funktionieren |
| Structural Design | Mechanische Systeme werden aus starren Bauteilen zusammengesetzt. | Faltet DNA-Stränge zu Boxen, Gelenken und Käfigen. | Ermöglicht den Aufbau präziser Nanostrukturen. |
| Motion Control | Zufällige Molekularbewegung stört das Verhalten von Maschinen im Nanobereich. | Steuerung von Bewegungen mithilfe von DNA-Reaktionen oder -Signalen. | Ermöglicht vorhersagbare molekulare Aktionen |
| medizinischen Gebrauch | Viele Therapien beeinträchtigen nach wie vor auch gesundes Gewebe. | Die Medikamente sollen gezielt an den erkrankten Zellzielen verabreicht werden. | Könnte die Präzision verbessern und gleichzeitig Nebenwirkungen reduzieren |
| Fertigungsmaßstab | Die Herstellung identischer DNA-Maschinen bleibt schwierig und kostspielig. | Entwicklung zuverlässiger, ertragreicher Bioproduktionsverfahren. | Unverzichtbar für den Einsatz in der Praxis jenseits von Laboren |
| Zukünftige Entwicklung | Konstruktionswerkzeuge und Simulationen sind auch heute noch unterentwickelt. | Nutzen Sie KI, um Design und Verhalten zu optimieren. | Könnte den Fortschritt in Medizin und Informatik beschleunigen |
Um die Bewegungen dieser Maschinen zu steuern, haben Wissenschaftler Systeme entwickelt, die es ihnen ermöglichen, sich vorhersagbar zu verhalten. Dazu gehören biochemische Reaktionen und physikalische Signale wie Wärme, Licht, Magnetfelder und elektrische Felder.
Bei der biochemischen Steuerung nutzen Forscher die DNA-Strangverdrängung. Dieses Verfahren ermöglicht die präzise Programmierung von Bewegungen mithilfe von „Treibstoff“- und „Struktur“-DNA-Sequenzen. Dabei verdrängt ein Strang den anderen und fungiert so als molekularer Schalter, der eine bestimmte Bewegung auslösen kann.
Allerdings birgt jede Methode auch Nachteile, sodass Wissenschaftler Präzision und Geschwindigkeit gegeneinander abwägen müssen.
Die chemische Steuerung bietet beispielsweise Präzision und Vielseitigkeit, erzeugt aber Abfallmoleküle und erfordert umfangreiche experimentelle Untersuchungen. Externe physikalische Signale hingegen wirken schnell, beeinflussen aber umliegende Systeme. Sie bewegen ganze Strukturen, ermöglichen jedoch nur schwer eine unabhängige Steuerung einzelner Gelenke.
Durch die Kombination dieser Strategien stellen Wissenschaftler ein Instrumentarium zur Verfügung, mit dem sich das Verhalten von DNA-Maschinen mit großer Präzision feinabstimmen lässt. Die Studie stellt fest, dass die Anwendungsmöglichkeiten dieser mikroskopischen Geräte weit über den Laborbereich hinausgehen.
Zunächst einmal können DNA-Roboter in der Präzisionsmedizin von immenser Bedeutung sein, wo sie als „Nano-Chirurgen“ im Körper fungieren können, indem sie erkrankte Zellen identifizieren und Therapien an diese Zellen abgeben.
In einem Beispiel mit einem DNA-Roboter wurde SARS-CoV-2 innerhalb einer halben Stunde mithilfe von vier flexiblen Fingern aus Speichelproben isoliert. Die Ergebnisse waren dabei genauso gut wie bei herkömmlichen Labortests. In einem anderen Fall transportierte der Roboter ein gerinnungshemmendes Medikament zu den Blutgefäßen von Tumoren bei Mäusen und gab es erst ab, nachdem es das Ziel erreicht hatte. Dies demonstriert sein Potenzial als autonomes Medikamentenverabreichungssystem.
DNA-Roboter können auch als programmierbare Vorlagen für die Anordnung von Materialien dienen und dadurch molekulare optische Geräte, Rechengeräte und ultradichte Datenspeichersysteme ermöglichen, die effizienter sind als die derzeitige Technologie.
DNA-Leitstrukturen, Nanopartikel und Lichtquellen wurden bereits zu geordneten Mustern angeordnet. In verwandten Experimenten haben Forscher außerdem chemische Markierungen auf synthetische DNA gedruckt und Bilder kodiert, ohne jede Base neu zu schreiben. Die Möglichkeiten mit diesen DNA-Maschinen sind also schlichtweg herausragend.
Natürlich befindet sich das alles noch in einem frühen experimentellen Stadium. Da sie noch weit von praktischen Anwendungen in der realen Welt entfernt sind, lassen sich diese DNA-Roboter am besten als Machbarkeitsnachweis verstehen. Die Realisierung dieser Maschinen steht tatsächlich vor mehreren Herausforderungen. Eine davon ist der Umfang.
Beim Übergang von großskaligen Systemen zum Nanobereich (∼100 nm, etwa 1/500 bis 1/1000 der Breite eines menschlichen Haares) wird die präzise Steuerung dieser Maschinen aufgrund der Brownschen Molekularbewegung, also der kleinen, zufälligen Bewegung von Nanopartikeln, und thermischer Schwankungen schwierig. Die Studie stellte fest:
„Obwohl die makroskopische Robotik wertvolle konzeptionelle und analytische Rahmenbedingungen bietet, erfordert die Übertragung ihrer Prinzipien auf die molekulare und nanoskalige Ebene eine grundlegende Neudefinition des mechanischen Designs und der Bewegungssteuerung unter stochastischen, thermodynamischen und biochemischen Randbedingungen.“
Deshalb sind viele der existierenden DNA-Roboterdesigns einfach und arbeiten isoliert. Auch ihre Nützlichkeit in komplexen realen Umgebungen ist begrenzt.
Zukünftige Systeme müssen jedoch skalierbar, rekonfigurierbar und funktional integriert sein, was die Anwendung fortschrittlicher Modularität und die Übertragung makroskopischer mechanischer Prinzipien auf die molekulare Ebene voraussetzt.
Hinzu kommt das Problem der Wissenslücken. Noch immer mangelt es Forschern an detaillierten Informationen und einem umfassenden Verständnis der mechanischen Eigenschaften von DNA-Strukturen. Computergestützte Modellierungs- und Simulationswerkzeuge zur Vorhersage des Verhaltens dieser Strukturen auf solch mikroskopischen Skalen sind noch nicht vollständig entwickelt.
Die Herstellung stellt ein weiteres Hindernis dar. Die Produktion identischer DNA-Maschinen in großem Maßstab ist für ihre praktischen Anwendungen notwendig, erfordert jedoch kostengünstige, ertragreiche und zuverlässige Methoden, die nach wie vor schwer zu realisieren sind.
Die Überwindung all dieser Hindernisse, so die Studie, erfordert die Zusammenarbeit verschiedener Disziplinen: Maschinenbau, Informatik, Medizin, Chemie und Biologie.
Konkret schlagen Wissenschaftler Lösungen vor wie die Weiterentwicklung von Bioproduktionsmethoden, die Schaffung standardisierter DNA-„Bausteinbibliotheken“ und den Einsatz von KI zur Verbesserung von Design und Simulation.
Deep Learning und LLMs bieten laut der Studie „transformative Möglichkeiten zur Weiterentwicklung des Designs und der Analyse von DNA-Maschinen“ sowie der Simulation und Dynamikanalyse. Die Technologie kann Strukturmuster aus großen Datensätzen aufdecken, Faltungswege vorhersagen, Sequenzkonfigurationen optimieren und die Designbewertung automatisieren, wodurch der Innovationszyklus deutlich beschleunigt wird.
Fortschritte in diesen Bereichen werden dazu beitragen, DNA-Roboter in größerem Maßstab einzusetzen und sie in praktische Anwendungen in Wissenschaft, Gesundheitswesen, Fertigung und darüber hinaus zu integrieren.
Investitionen in DNA-Robotiktechnologie
In der Welt der medizinischen Robotik, Illumina, Inc. (ILMN ) Das Unternehmen zeichnet sich durch seine Kernkompetenz in DNA-Technologien und seine starke Positionierung in der genomgestützten Medizin aus. Obwohl es selbst keine DNA-Roboter entwickelt, ist es ein wichtiger Wegbereiter für das gesamte Ökosystem, das solche Innovationen ermöglicht.
Als weltweit führendes Unternehmen im Bereich der DNA-Sequenzierung stellt es die grundlegenden Werkzeuge für die Forschung an DNA-basierten Systemen bereit, darunter DNA-Nanotechnologie und Robotik. Es ist zudem maßgeblich am Wandel hin zu personalisierter und molekularer Medizin beteiligt.
Die Produkte des Unternehmens finden Anwendung in Forschung und Klinik sowie in der Onkologie, den Biowissenschaften, der Reproduktionsmedizin, der Landwirtschaft und weiteren Bereichen. Zu den Kunden zählen akademische Einrichtungen, Genomforschungszentren, Krankenhäuser, staatliche Labore, kommerzielle molekulardiagnostische Labore, Biotechnologie-, Pharma- und Verbrauchergenomikunternehmen.
Illuminas Ziel ist es, die menschliche Gesundheit durch die Erschließung des Potenzials des Genoms zu verbessern. Erst im letzten Monat kündigte Illumina eine strategische Zusammenarbeit mit Veritas Genetics an, um die Sequenzierung des gesamten Genoms über Versicherungssysteme in die alltägliche Gesundheitsversorgung zu integrieren.
Diese Zusammenarbeit fördert ein integriertes Datenökosystem zur Weiterentwicklung von Forschung, Wirkstoffentwicklung und Optimierung klinischer Studien. Noch wichtiger ist jedoch, dass sie einen Paradigmenwechsel von der Behandlung von Krankheiten hin zu deren Vorhersage und Prävention mithilfe genetischer Daten markiert.
„Die Genomik rückt im Gesundheitswesen immer stärker in den Vordergrund – von der Krankheitsdiagnose hin zur Prävention“, sagte Rami Mehio, General Manager BioInsight bei Illumina. „Durch die Kombination der Sequenzierungs- und Informatik-Infrastruktur von Illumina mit den patientenorientierten Berichten von Veritas stellt diese Zusammenarbeit einen wichtigen Schritt dar, um die präventive Genomik nutzbar, zugänglich und in die alltägliche Gesundheitsversorgung zu integrieren.“
Ein paar Monate zuvor hatte Illumina den Billion Cell Atlas vorgestellt, den weltweit größten Datensatz zur genomweiten genetischen Perturbation, der DNA-Roboter praktisch und programmierbar machen könnte.
Dieser riesige Datensatz, der mithilfe von CRISPR und Sequenzierung erstellt wurde, bildet ab, wie Milliarden von Zellen auf genetische Veränderungen reagieren. Die erste Phase des dreijährigen Programms des Unternehmens, einen Atlas mit fünf Milliarden Zellen zu erstellen – die bisher umfassendste Karte der menschlichen Krankheitsbiologie –, dient dem Training von KI-Modellen und der Beschleunigung der Wirkstoffforschung in Zusammenarbeit mit Merck, AstraZeneca und Eli Lilly and Company.
„Wir sind überzeugt, dass der Zellatlas eine Schlüsselentwicklung darstellt, die es uns ermöglichen wird, KI für die Wirkstoffforschung deutlich auszuweiten“, sagte Jacob Thaysen, CEO von Illumina. „Wir schaffen eine beispiellose Ressource für das Training der nächsten Generation von KI-Modellen für die Präzisionsmedizin und die Identifizierung von Wirkstoffzielen. Dies wird letztendlich dazu beitragen, die biologischen Mechanismen hinter einigen der verheerendsten Krankheiten der Welt zu entschlüsseln.“
(ILMN )
Trotz dieser positiven Entwicklungen notieren die Aktien von Illumina, die eine Marktkapitalisierung von 19.5 Milliarden US-Dollar aufweisen, bei 127.74 US-Dollar, was einem Anstieg von 74 % im vergangenen Jahr entspricht. Der Gewinn je Aktie (TTM) beträgt 5.48 US-Dollar, das Kurs-Gewinn-Verhältnis (TTM) 23.32.
Was die Finanzstärke von Illumina betrifft, so meldete das Unternehmen für das vierte Quartal 2025 einen Umsatz von 1.16 Milliarden US-Dollar, ein Plus von 5 % gegenüber dem vierten Quartal 2024. Die operative Marge nach GAAP betrug 17.4 %, die operative Marge nach Non-GAAP 23.7 %. Der verwässerte Gewinn je Aktie (EPS) nach GAAP lag bei 2.16 US-Dollar, der verwässerte Gewinn je Aktie nach Non-GAAP bei 1.35 US-Dollar.
In diesem Zeitraum beliefen sich die Investitionsausgaben auf 54 Millionen US-Dollar, während der operative Cashflow 321 Millionen US-Dollar betrug. Zum Jahresende verfügte das Unternehmen über liquide Mittel und kurzfristige Anlagen in Höhe von 1.63 Milliarden US-Dollar.
Im Geschäftsjahr 2025 erzielte Illumina einen Umsatz von 4.34 Milliarden US-Dollar. Die operative Marge nach GAAP betrug 18.6 %, die operative Marge nach Non-GAAP 23.1 %. Der verwässerte Gewinn je Aktie (EPS) nach GAAP lag bei 5.45 US-Dollar, der verwässerte Gewinn je Aktie (EPS) nach Non-GAAP bei 4.84 US-Dollar.
Die Investitionsausgaben beliefen sich im vergangenen Jahr auf 148 Millionen US-Dollar, der operative Cashflow betrug 1.1 Milliarden US-Dollar und der freie Cashflow 931 Millionen US-Dollar.
Mit Blick auf den „starken Abschluss des Jahres 2025“ sagte Thaysen, dies markiere „eine Rückkehr zum Wachstum durch disziplinierte Umsetzung unserer Strategie“, wobei die Dynamik in der zweiten Hälfte des letzten Jahres aufgebaut wurde, insbesondere durch die zunehmende Nutzung von NGS-basierten Tests auf klinischen Märkten.
Bemerkenswert ist, dass Illumina in China Fortschritte erzielt hat, da das Exportverbot für seine Sequenziergeräte aufgehoben wurde. Das Unternehmen steht jedoch weiterhin auf der Liste unzuverlässiger Unternehmen (UEL), weshalb für den Kauf von Geräten Genehmigungen erforderlich sind.
Für das laufende Jahr erwartet Illumina einen Umsatzanstieg von 4 % bis 6 % auf 4.5 bis 4.6 Milliarden US-Dollar. Dieses Wachstum beinhaltet einen positiven Effekt von 1.5 % bis 2 % aus der kürzlich abgeschlossenen Übernahme von SomaLogic, wodurch das Multiomics-Portfolio des Unternehmens erweitert und seine Position im Bereich der NGS-basierten Proteomik gestärkt wird.
Aktuelle Aktiennachrichten und Entwicklungen zu Illumina, Inc. (ILMN)
Fazit
Roboter haben die Möglichkeiten von Maschinen grundlegend verändert. Sie steigern Produktivität, Sicherheit und Forschung in zahlreichen Bereichen. Von der industriellen Automatisierung bis zur Planetenforschung – die kontinuierliche Weiterentwicklung von Robotern verdeutlicht einen umfassenderen Trend hin zu leistungsfähigeren Systemen, die immer tiefer in unseren Alltag integriert werden.
In der Medizin ermöglicht das Aufkommen biologisch kompatibler Roboter wie DNA-basierter Systeme eine beispiellose Präzision bei der Medikamentenverabreichung und der gezielten Bekämpfung von Viren.
Wichtiger noch: Diese Systeme versprechen nicht nur präzisere Behandlungen und verbesserte Patientenergebnisse, sondern auch eine neue Methode, um Prozesse auf molekularer Ebene zu untersuchen und durch DNA-gesteuerte Assemblierung kleinere, leistungsfähigere Geräte zu bauen.
Obwohl erhebliche Herausforderungen hinsichtlich Skalierbarkeit, Stabilität und Langzeitsicherheit bewältigt werden müssen, bevor diese Technologien von der Laborforschung in die klinische Praxis überführt werden können, sind die potenziellen Vorteile beträchtlich. Und da die Robotik immer kleiner und leistungsfähiger wird, kann sie eine Zukunft ermöglichen, in der Medizin intelligent von innen heraus ausgeführt wird.
Klicken Sie hier, um zu erfahren, ob KI unsere DNA umschreiben kann.
Referenzen
1. Xu, N., Zhang, SmartBot (2026). https://doi.org/10.1002/smb2.70029