التكنولوجيا الحيوية
الجيل القادم من تقنية CRISPR يعزز الدقة في العلاج الجيني
تلتزم Securities.io بمعايير تحريرية صارمة، وقد تتلقى تعويضات عن الروابط المُراجعة. لسنا مستشارين استثماريين مُسجلين، وهذه ليست نصيحة استثمارية. يُرجى الاطلاع على كشف التابعة لها.

جعل تحرير الجينات أكثر دقة
حتى وقت قريب، كانت التعديلات الجينية بدائية إلى حد ما، إذ كانت تتضمن إدخال تسلسل جيني جديد بشكل عشوائي في الكائنات الحية المستهدفة.
كانت طريقة الإدخال مدمرة للغاية أيضًا. ونتيجةً لذلك، لم تُعدّل وراثيًا إلا البكتيريا والنباتات بشكل روتيني، وكان أي تعديل جيني في كائنات حية مثل الثدييات (بما في ذلك البشر) معقدًا ومكلفًا وبطيئًا.
لقد تغير هذا جزئيًا مع تقنية CRISPR، التي فتحت الطريق فجأة لتحرير الجينات بدقة وضبط، مما أدى إلى الموافقة على أول علاج جيني للأمراض الوراثية البشرية في نهاية عام 2023.
ومع ذلك، فإن تقنية CRISPR ليست مثالية حتى الآن، مما يؤدي في بعض الأحيان إلى تعديلات جينية غير مرغوب فيها.
ربما تغير هذا الأمر للتو مع الاكتشاف الرائد الذي توصل إليه ثلاثة باحثين من معهد ماساتشوستس للتكنولوجيا.
أعلنوا عن طريقة جديدة تسمح بتحسين موثوقية تحرير الجينات بشكل جذري، مما يفتح الطريق أمام ابتكار علاجات جديدة.
وقد نشروا نتائجهم في المجلة العلمية المرموقة Nature1، تحت عنوان "محررات أولية مُهندسة مع الحد الأدنى من الأخطاء الجينومية".
من تقنية CRISPR القياسية إلى تقنية التحرير الأولية
منذ اعتماد أولى العلاجات القائمة على تقنية كريسبر-كاس9، لم تعد فكرة تعديل جينومات المرضى بشكل موثوق لعلاجهم ضربًا من الخيال العلمي. ومع ذلك، فإن تقنية كريسبر لا تُعدّل الجين المستهدف دائمًا بالطريقة التي ينوي العلماء القيام بها.
يتكون نظام CRISPR من إنزيم يسمى Cas9 والذي يمكنه قطع الحمض النووي مزدوج السلسلة في نقطة معينة، إلى جانب الحمض النووي الريبوزي المرشد الذي يخبر Cas9 بمكان القطع.
وقد قام الباحثون بتكييف هذا النهج لقطع تسلسلات الجينات الخاطئة أو إدراج تسلسلات جديدة، باتباع نموذج الحمض النووي الريبي.
منذ عام ٢٠١٩، نشر باحثو معهد ماساتشوستس للتكنولوجيا (MIT) مفهومًا جديدًا يُسمى التحرير الأولي، وهو أكثر دقة من تحرير الجينات التقليدي بتقنية كريسبر-كاس٩. ونتيجةً لذلك، تقلّ آثاره غير المقصودة، ويقلّ احتمال تسببه في مشاكل صحية إضافية للمرضى الذين غالبًا ما يكونون ضعفاء أصلًا.
تستخدم عملية التحرير الأولي إنزيم Cas9 المعدل المدمج مع إنزيم النسخ العكسي، مما يسمح له بإجراء جميع التعديلات الجينية الأساسية الممكنة، بالإضافة إلى عمليات الإدراج والحذف الصغيرة للتسلسلات الجينية.
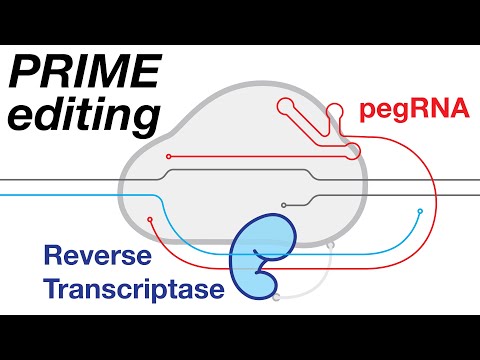
وعلى المدى الطويل، من المتوقع أن يصبح التحرير الأولي هو النسخة المطورة والأكثر موثوقية من التحرير الجيني القائم على تقنية CRISPR.

المصدر بنيامين ماكليود
على سبيل المثال، تم استخدام المحررين الأوليين بنجاح في عام 2025 لعلاج مريض مصاب بمرض الحبيبات المزمن (CGD)، وهو مرض وراثي نادر يؤثر على خلايا الدم البيضاء.
"من حيث المبدأ، يمكن استخدام هذه التقنية في نهاية المطاف لمعالجة مئات الأمراض الوراثية عن طريق تصحيح الطفرات الصغيرة مباشرة في الخلايا والأنسجة."
فيكاش تشوهان - معهد كوخ لأبحاث السرطان التكاملية التابع لمعهد ماساتشوستس للتكنولوجيا
لكنها كانت بحاجة إلى بعض التحسين قبل أن تصبح جاهزة للاستخدام في خلايا وأجسام البشر.
كيف يُحسّن التحرير الأولي دقة إدخال الحمض النووي
تقوم عملية التحرير الأولي بقطع أحد الخيوط التكميلية لتسلسل الحمض النووي المستهدف، مما يفتح غطاءً يمكن إدخال تسلسل جديد فيه.
ومع ذلك، بمجرد نسخ التسلسل الجديد، فإنه يجب أن يتنافس مع خيط الحمض النووي القديم من أجل دمجه في الجينوم.
إذا تفوقت السلسلة القديمة على السلسلة الجديدة، فقد يتم دمج الشريحة الإضافية من الحمض النووي التي تم إنشاؤها حديثًا والمعلقة عن طريق الخطأ في مكان آخر، مما يؤدي إلى حدوث أخطاء.
وقد تؤدي مثل هذه الأخطاء في نهاية المطاف إلى الإصابة بالسرطان عن طريق إدخال نفسها بشكل عشوائي في الجينوم، وهو خطر واضح يجب الحد منه.
مع أحدث إصدار من محرري التحرير الأساسيين، يتراوح معدل الخطأ هذا من خطأ واحد لكل سبع تعديلات إلى خطأ واحد لكل 121 تعديلاً لأوضاع التحرير المختلفة، وهو ما يزال مرتفعاً للغاية.
"إن التقنيات التي لدينا الآن أفضل بكثير من أدوات العلاج الجيني السابقة، ولكن هناك دائمًا فرصة لهذه العواقب غير المقصودة"
فيكاش تشوهان - معهد كوخ لأبحاث السرطان التكاملية التابع لمعهد ماساتشوستس للتكنولوجيا
قفزة كبيرة في موثوقية التحرير الرئيسي
في عام 2023، اكتشف باحثو معهد ماساتشوستس للتكنولوجيا أن بعض الإصدارات المتحولة من بروتين Cas9 المستخدم في التحرير الأولي قد تقوم أحيانًا بإجراء قطع على قاعدة واحدة أو قاعدتين أبعد على طول تسلسل الحمض النووي، بدلاً من أن تكون دائمًا في نفس المكان.
وقد أدى هذا إلى جعل خيوط الحمض النووي القديمة أقل استقرارًا، وبالتالي تتدهور، مما يجعل من السهل دمج الخيوط الجديدة دون إدخال أي أخطاء.
وفي هذه الدراسة الجديدة التي أجريت عام 2025، حدد الباحثون طفرات متعددة في Cas9 والتي حددت طفرات Cas9 التي خفضت معدل الخطأ إلى 1/20 من قيمته الأصلية.
وعند الجمع بين هذه الطفرات بشكل مصطنع في بروتين Cas9 واحد، انخفض معدل الخطأ إلى 1/36 من الكمية الأصلية.
"تتناول هذه الورقة نهجًا جديدًا لتحرير الجينات لا يُعقّد نظام التسليم ولا يضيف خطوات إضافية، ولكنه يؤدي إلى تحرير أكثر دقة مع عدد أقل من الطفرات غير المرغوب فيها."
فيليب شارب - معهد كوخ لأبحاث السرطان التكاملية التابع لمعهد ماساتشوستس للتكنولوجيا
ولم يكتفوا بذلك، بل استخدموا أيضًا نظام تحرير أولي يحتوي على بروتين يرتبط بالحمض النووي الريبي (RNA) والذي يعمل على تثبيت نهايات قالب الحمض النووي الريبي بكفاءة أكبر.
تم تسمية النسخة النهائية من مجموعة أدوات تحرير الجينات الخاصة بهم باسم vPE، وكان معدل الخطأ فيها 1/60 فقط من النسخة الأصلية، أو 101-543 تعديلًا فقط، اعتمادًا على أوضاع التحرير المستخدمة.
مرر للتمرير →
| إصدار المحرر الرئيسي | معدل الخطأ التقريبي | التحسين مقابل الأصل |
|---|---|---|
| المحرر الرئيسي الأصلي | خطأ واحد لكل 7-121 تعديلًا | خط الأساس |
| متغيرات Cas9 المتحولة | معدل الخطأ الأصلي 1/20–1/36 | حتى 36× أكثر دقة |
| vPE (مستقر الحمض النووي الريبي) | معدل الخطأ الأصلي 1/60 | حتى 60× أكثر دقة |
الخطوات التالية
كانت هناك عقبة أخرى أمام تحرير الجينات تتمثل في توصيل بروتينات تحرير الجينات والحمض النووي/الحمض النووي الريبوزي إلى داخل نواة الخلايا المستهدفة، أو استهداف أنسجة محددة فقط في الجسم.
وسيكون هذا هو محور التركيز التالي للباحثين، خاصة وأن تقنيات التحرير الأولية محدودة بسبب سوء التسليم مقارنة بأنظمة CRISPR-Cas9 "التقليدية" الأصغر والأبسط.
ويعتقدون أيضًا أن هذه الأداة لديها القدرة على تسريع التقدم في التكنولوجيا الحيوية بشكل عام، وليس فقط فيما يتعلق بعلاجات تحرير الجينات.
أولا، يمكن نشر التقنية واكتشاف أن تعديل بروتين Cas9 يمكن أن يحسن من موثوقيته في جميع تقنيات تحرير الجينات المستندة إلى CRISPR، وليس فقط التحرير الأولي.
ثانيًا، قد يُشكّل هذا دفعة قوية لمشاريع بحثية أخرى تستخدم تعديل الجينات والجينوم كأداة بحثية. على سبيل المثال، إيجاد إجابات حول كيفية تطور الأنسجة، وكيفية تطور مجموعات الخلايا السرطانية، وكيفية استجابة الخلايا للعلاج الدوائي.
"يتم استخدام محرري الجينوم على نطاق واسع في مختبرات الأبحاث.
لذا فإن الجانب العلاجي مثير للاهتمام، ولكننا متحمسون حقًا لرؤية كيف سيبدأ الناس في دمج محررينا في سير عملهم البحثي.
فيكاش تشوهان - معهد كوخ لأبحاث السرطان التكاملية التابع لمعهد ماساتشوستس للتكنولوجيا
أخيرًا، ربما لم تُكتشف جميع الطفرات التي تُحسّن موثوقية Cas9 في هذه الدراسة. لذا، قد يُسفر المزيد من التحليل والتحسين لهذا المفهوم الجديد عن نتائج أفضل في المستقبل.
الاستثمار في تحرير الجينات
البورشيد
(ILMN )
وعلى الرغم من أنه تم تأسيس ما يخص -omics أخرى في multiomics (البروتينات، النسخيات، وما إلى ذلك) إن هذه الاكتشافات مهمة، وترتبط جميعها تقريبًا بطريقة أو بأخرى بعلم الجينوم، وهو "دليل التعليمات" الأساسي لكل خلية حية.
وأكبر مُصنِّع لأجهزة تسلسل الجينوم بلا منازع هي شركة إيلومينا. تُركِّز الشركة على قراءة التسلسلات الجينية القصيرة، وهي التقنية المُستخدمة للكشف عن السرطان. ولديها حاليًا أكثر من 22,000 جهاز تسلسل مُثبَّت في 165 دولة.
يُستخدم حوالي نصف المواد الاستهلاكية لأجهزة التسلسل الجيني من شركة "إيلومينا" في التطبيقات السريرية، بينما يُستخدم النصف الآخر في مختبرات الأبحاث العامة والخاصة. أما في التطبيقات السريرية، فيأتي نصف الطلب من علم الأورام.

المصدر البورشيد
وبما أن علم الجينوم وعلم الجينوم المتعدد أصبحا مركز عملية اكتشاف الأدوية، فضلاً عن تشخيص السرطان، فمن المتوقع أن يكون الطلب على معدات Illumina مرتفعاً.
وتتوقع الشركة أن ينمو الطلب على تقنية تسلسل الجيل التالي (NGS) بنسبة 18% CAGR للتطبيقات السريرية و6% CAGR للأبحاث، مما يعزز إجمالي السوق المستهدفة للقطاع (TAM) من 100 مليار دولار للتطبيقات السريرية إلى 25 مليار دولار للأبحاث بحلول عام 2033.

المصدر البورشيد
كان لشركة Illumina تاريخ معقد مع شركة Grail للخزعة السائلة (GRAL -0.36٪)، والتي كانت شركة فرعية من شركة Illumina، وتم الاستحواذ عليها مرة أخرى في وقت لاحق، والآن أجبرتها سلطات المنافسة في الولايات المتحدة والاتحاد الأوروبي على العودة إلى شركة فرعية.
وبعد التغلب على هذه المشكلة، قد تستأنف شركة إيلومينا نموها على المدى الطويل وارتفاع سعر أسهمها، خاصة وأن اختبارات خزعة السوائل التي تجريها شركة جرايل من المرجح أن تستمر في الاعتماد على أجهزة تسلسل إيلومينا.
وفي الوقت نفسه، سوف تؤدي المزيد من العلاجات الجينية أيضًا إلى زيادة استخدام أجهزة تسلسل Illumina في كل من الإعدادات البحثية والسريرية.
(يمكنك أيضًا القراءة تحليل أكثر تفصيلاً لأعمال Illumina وتقنياتها المستقبلية وتاريخها في تقرير الاستثمار المخصص.)
أحدث أخبار وتطورات أسهم Illumina (ILMN)
الدراسة المرجعية
1. تشوهان، نائب الرئيس، شارب، PA ولانجر، R. محررات أولية مُهندسة مع الحد الأدنى من الأخطاء الجينومية. الطبيعة (2025). https://doi.org/10.1038/s41586-025-09537-3











