التكنولوجيا الحيوية
هل يمكن أن يكون CRISPR هو السلاح الخارق القادم ضد الفيروسات؟
تلتزم Securities.io بمعايير تحريرية صارمة، وقد تتلقى تعويضات عن الروابط المُراجعة. لسنا مستشارين استثماريين مُسجلين، وهذه ليست نصيحة استثمارية. يُرجى الاطلاع على كشف التابعة لها.

إمكانات كريسبر تتجاوز تحرير الجينات
منذ اكتشافها، فازت تقنية CRISPR ("التكرارات القصيرة المتناظرة المتجمعة بانتظام") بجائزة نوبل في الطب. جائزة نوبل 2020 في الكيمياءلقد أحدثت ثورة في الطب والتكنولوجيا الحيوية.

المصدر جائزة نوبل
وذلك لأن CRISPR هي الطريقة الأولى لتحرير الجينات التي تسمح باستهداف دقيق للغاية لتسلسل جيني محدد، مما يسمح بتصحيح الأخطاء الجينية إما المختبر or بإختبارin vivo دون المخاطرة بالطفرات غير المرغوب فيها.
وهذا أمر مهم لأن إدراج الجينات غير الموجهة يرتبط بمشاكل كبيرة، ولا سيما مخاطر الإصابة بالسرطان، مما يجعل استخدامها العلاجي صعبًا ومثيرًا للجدل.
يمكن استخدام CRISPR بطرق متعددة لمقاطعة جين موجود بالفعل، أو حذف تسلسل معين، أو تحرير/إدراج التسلسل الجيني الصحيح.

المصدر العلاجات كريسبر
وقد تحول هذا إلى اختراق طبي مع موافقة إدارة الغذاء والدواء الأمريكية على أول علاج قائم على تقنية كريسبر في عام 2023، التي وضعتها العلاجات كريسبر (CRSP ) لأمراض الدم الوراثية (اتبع الرابط للحصول على تقرير مخصص حول CRISPR Therapeutics).
مع ذلك، فإن التحرير الجيني الدقيق الذي يتحكم فيه الإنسان ليس ما استُخدمت فيه تقنية كريسبر في الطبيعة. فهي، في المقام الأول، أداة مضادة للفيروسات تستخدمها البكتيريا للنجاة من هجمات الفيروسات.
وهذا يطرح تساؤلاً حول إمكانية استخدام تقنية كريسبر بنفس الطريقة لعلاج الفيروسات البشرية، وخاصةً تلك التي يصعب مكافحتها باللقاحات أو العلاجات المضادة للفيروسات.
هذه هي الفكرة التي بحثها باحثون في جامعة آزاد الإسلامية (إيران)، وجامعة سمنان للعلوم الطبية (إيران)، وجامعة شهيد بهشتي للعلوم الطبية (إيران)، وجامعة شهرود للعلوم الطبية (إيران)، وجامعة بيرغن (النرويج).
وقد نشروا نتائجهم في مراجعة منهجية للأبحاث الجارية في هذا المجال في مجلة MDPI، تحت عنوان "التقدم في تقنية كريسبر لعلاجات مضادة للفيروسات: تعديل الجينوم كعلاج محتمل للعدوى الفيروسية المزمنة".
الأصول الطبيعية لتقنية كريسبر كوسيلة دفاع فيروسية
تتعرض معظم البكتيريا لتهديد مستمر من الفيروسات المتخصصة بمهاجمتها، والتي تُسمى العاثيات (وتُسمى حرفيًا "آكلات البكتيريا"). تعمل العاثيات عن طريق الهبوط على البكتيريا وحقنها بمادتها الوراثية، لتكاثر المزيد من الفيروسات.

المصدر علم الجينوم المبتكر
يتم اشتقاق كل تسلسل جيني CRISPR موجود داخل CRISPR بكتيري فردي من جزء DNA من بكتيريا عاثية سبق أن أصابت بدائية النواة أو أحد أسلافها.
بهذه الطريقة، يستطيع نظام CRISPR التعرف على المادة الوراثية للبكتيريا، وقطعها إلى قطع قبل أن تتمكن من التكاثر إلى جزيئات فيروسية جديدة.
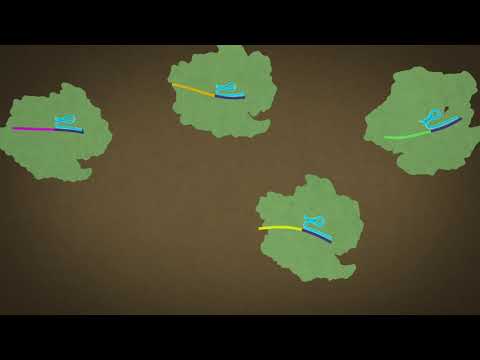
يُشكّل هذا نوعًا من "المناعة المكتسبة" للبكتيريا ضد فيروسات العاثيات. وُجدت تقنية كريسبر في حوالي 50% من الجينومات البكتيرية المُسَلَّسة.
بالنظر إلى مدى انتشار أنظمة CRISPR، وأهميتها ضد العدوى الفيروسية للبكتيريا، هل يمكن استخدام هذه الطريقة لعلاج الفيروسات لدى البشر أيضًا؟
استهداف العدوى المزمنة باستخدام CRISPR
لماذا العدوى المزمنة؟
عند مناقشة العدوى الفيروسية، تُعدّ العدوى المزمنة الشغل الشاغل للأطباء. ويشمل ذلك فيروسات مثل فيروس نقص المناعة البشرية (HIV) أو التهاب الكبد الوبائي (C).
إن المشكلة الخاصة بهذه الأمراض والتي تجعلها تتجنب العلاج والجهاز المناعي للجسم هي أنها يمكن أن تصبح خاملة، مع بقاء المادة الوراثية الفيروسية مدمجة في الخلية، وفي بعض الأحيان تظل صامتة لسنوات.
في بعض الأحيان، يتحول الفيروس المسبب للمرض إلى وضع غير نشط لا يمكن نسخه، مما يثير مشكلة.
لا يقتصر الأمر على عدم قدرة الجهاز المناعي البشري على مهاجمة هذه المستودعات الكامنة، بل تفشل الأدوية المضادة للفيروسات القهقرية أيضًا في التأثير على هذه الأجزاء غير المنسوخة. يمكن لبعض مستودعات فيروس نقص المناعة البشرية من النوع 1 البقاء على قيد الحياة لمدة تصل إلى 60 عامًا في الخلايا التائية CD4+.
هناك عدة طرق يمكن من خلالها استخدام تقنية CRISPR لاستهداف هذه الالتهابات الفيروسية المزمنة.
هل يمكن لـCRISPR أن يساعد في علاج فيروس نقص المناعة البشرية/الإيدز؟
أحد الخيارات هو الهندسة الوراثية، لإنتاج خلايا بشرية تفتقر إلى المستقبلات اللازمة لنجاح العدوى الفيروسية. في حالة الإيدز/فيروس نقص المناعة البشرية، تُصبح الخلايا التائية المناعية المعدلة CD4+، الخالية من المستقبلات المشتركة CCR5 وCXCR4، مقاومة للفيروس، ويمكنها منع دخوله.
ويبدو أن هذا النهج يعمل في المختبر، ولكن سيتطلب دراسات مكثفة على الحيوانات، ثم تجارب على البشر لتحديد ما إذا كان فعالاً وآمناً بما يكفي ليصبح علاجاً موثوقاً به لهذا المرض.
تم النظر في نفس طريقة تعديل الخلايا البشرية لفيروس التهاب الكبد الوبائي سي. إن تقنية CRISPR-Cas13a التي تستهدف موقع دخول الفيروس إلى خلايا الكبد تمنع تكاثر الفيروس بشكل فعال مع أضرار محدودة للغاية لخلايا الكبد، أقل بكثير من الأضرار التي يسببها الفيروس.
كريسبر مقابل عدوى التهاب الكبد الوبائي ب الكامنة
على غرار فيروس نقص المناعة البشرية، يشكل فيروس التهاب الكبد B خزانًا فيروسيًا كامنًا باستخدام "الحمض النووي الدائري المغلق تساهميًا" (cccDNA) في خلايا الكبد.
أشارت الدراسات التي أجريت على الخلايا المزروعة إلى أن أنظمة CRISPR التي تستهدف التسلسلات المحفوظة في جينوم التهاب الكبد B يمكنها بنجاح تقليل 98٪ من مادة الحمض النووي لالتهاب الكبد B.
مكافحة فيروس الورم الحليمي البشري باستخدام CRISPR
فيروس الورم الحليمي البشري (HPV) هو فيروس ينتقل عن طريق الاتصال الجنسي، ويمكن أن يسبب آفات سرطانية قد تتحول لاحقًا إلى سرطان، ليس فقط في عنق الرحم، بل أيضًا في أعضاء أخرى. كما يمكن أن يصبح هذا الفيروس خاملًا.
هناك بعض اللقاحات ضد فيروس الورم الحليمي البشري، ولكنها لا تغطي جميع أنواع فيروس الورم الحليمي البشري، ولا يمكنها المساعدة في علاج العدوى الموجودة مسبقًا.
يمكن لأنظمة CRISPR رفع مستوى pRb، وهو بروتين مثبط للورم المضيف، مما يمنع نمو خلايا فيروس الورم الحليمي البشري الإيجابية ويمنع نشاطها السرطاني.
استخدام تقنية كريسبر لمعالجة فيروس إبشتاين بار (EBV)
فيروس إبشتاين بار، أو EBV، هو فيروس يصيب الخلايا المناعية (الخلايا الليمفاوية B) ويسبب مرض وحيدات النوى المعدي، وفي بعض الأحيان يمكن أن يتطور إلى سرطانات خبيثة، مثل ليمفوما بوركيت.
وهنا أيضا، يمكن لتعديل الخلايا المناعية أن يمنع تطورها نحو السرطان، وبالتالي قمع أسوأ تأثيرات فيروس إبشتاين بار بشكل فعال.
كريسبر مقابل الأساليب التقليدية لمكافحة الفيروسات
وكما رأينا مع جائحة كوفيد الأخيرة، فإن المشكلة المتكررة في اللقاحات هي كيفية استهداف جزء من الفيروس يكون مستقراً وثابتاً بما يكفي بين السلالات حتى يظل اللقاح فعالاً على الرغم من الطفرات السريعة.
ويرجع ذلك إلى أن الفيروسات ماهرة للغاية في تعديل بروتينات سطحها، وهي البروتينات الوحيدة التي يمكن للأجسام المضادة التي تنتجها اللقاحات الوصول إليها.
في المقابل، يمكن للطرق المعتمدة على CRISPR-Cas13d استهداف التسلسلات الجينية المحفوظة التي تشفر بروتين الغلاف وبوليميراز الحمض النووي الريبي، والتي تعد ضرورية لتكاثر الفيروس.
ومن خلال التركيز على هذه المناطق المحفوظة، يهدف PAC-MAN إلى توفير فعالية واسعة النطاق ضد سلالات الفيروس المختلفة وحتى عبر الفيروسات ذات الصلة.
ويمكن استخدام نفس الطريقة لفيروسات الإنفلونزا، والتي لديها القدرة على التحور باستمرار والتهرب من اللقاحات الموجودة.
على سبيل المثال، تم استهداف ما يصل إلى 92% من سلالات الأنفلونزا A المعروفة بنجاح باستخدام ستة crRNA فقط، وتم تحقيق نجاح مماثل مع SARS-CoV-2 باستخدام 22 crRNA.
علاجات كريسبر المضادة للفيروسات: التوقعات المستقبلية والقيود
حتى لو كان نظام كريسبر قادرًا على التكيف مع الطفرات، فهذا ليس مضمونًا تمامًا، كما يُثبت التكيف المستمر للعاثيات مع أنظمة كريسبر الطبيعية. لذا، فبينما قد تُمثل هذه الأساليب تقدمًا طبيًا كبيرًا، فمن غير المرجح أن تكون حلًا سحريًا أيضًا.
يُعدّ التعديل غير المستهدف للجينوم البشري أيضًا خطرًا، خاصةً مع أنظمة CRISPR-Cas9، والذي قد يُسبب في النهاية طفرةً أو سميةً للعلاج. وقد كان هذا الأمر أقل إثارةً للقلق في العلاج الجيني للأمراض الوراثية القاتلة التي لا علاج لها، مما أدى إلى الموافقة مؤخرًا على هذه العلاجات الجينية.
بالنسبة للأمراض المعدية في أعداد أكبر من السكان، قد تتخذ إدارة الغذاء والدواء موقفا أكثر صرامة ونهجا أكثر حذرا، مما يؤدي إلى إبطاء الطريق نحو تسويق هذه العلاجات.
كما أن نظام توصيل نظام كريسبر إلى الخلايا المضيفة ليس بالأمر الهيّن. فالنواقل الفيروسية أو الجسيمات النانوية قد تُحدث تفاعلات مناعية غير مرغوب فيها أو تستهدف أعضاءً أخرى غير الأعضاء المطلوبة.
إن التقدم في علاج CRISPR، من خلال استخدام إصدارات أخرى غير Cas9 (مثل CRISPR-Cas12a)، أو ناقلات جديدة يتحملها جسم الإنسان بشكل أكبر، سوف يفيد أيضًا تقدم علاجات CRISPR المضادة للفيروسات.
وبالإضافة إلى ذلك، فإن الطرق الجديدة مثل استخدام Cas13، التي تستهدف الحمض النووي الريبي الفيروسي دون الإضرار بالحمض النووي للمضيف، مناسبة بشكل خاص للاستجابة السريعة ضد فيروسات الحمض النووي الريبي مثل SARS-CoV-2.
الاستثمار في ابتكار CRISPR
إديتاس
(EDIT )
تأسست شركة Editas على يد جينيفر دودنا، إحدى مكتشفات CRISPR-Cas9. بدأت Editas العمل على Cas9، لكنها تُركز الآن على نسخة خاصة من Cas12a، وهي نسخة هندسية من Cas12a: AsCasXNUMXa.
يمكنك قراءة المزيد عن خصائص Cas12a الفريدة في مقالتنا المخصصة "ما هو كريسبر-Cas12a2؟ & لماذا يهم؟".

المصدر إديتاس
يمكنك أيضًا قراءة نظرة عامة على جميع شركات جينيفر دودنا في المقالة المقابلة "أفضل شركات جنيفر دودنا التي يجب مشاهدتها".
تركز شركة Editas على مرض فقر الدم المنجلي (SCD) والثلاسيميا بيتا، 2 مرض حيث خسر السباق للحصول على الموافقة العلاجية الأولى أمام المنافسين CRISPR Therapeutics وBlueBirdBio.
بشكل عام برنامج SCD (تمت إعادة تسميته مؤخرًا إلى Reni-Cell) تم تأجيلها عدة مرات، مما أثار القلق بين المستثمرين، ومنذ ذلك الحين تم التركيز مرة أخرى على العلاج الحيوي لتمييزها عن علاجات SCD المعتمدة بالفعل.
ومع ذلك، تمتلك شركة Editas براءات اختراع مهمة على CRISPR-Cas12، والتي استخدمها الباحثون في جامعة نيو ساوث ويلز، أستراليا. لتطوير اختبار شريط كوفيد-19، مما يوضح إمكانات التكنولوجيا بما يتجاوز تحرير الجينات.
تحرير أيضا وقعت في عام 2023 صفقة بقيمة 50 مليون دولار مع شركة Vertex لاستخدام الملكية الفكرية Cas9 الخاصة بشركة Editas.
وتركز شركة Editas على إصدارات أخرى من CRISPR غير CRISPR-Cas9 "الكلاسيكي"، وقد يكون لحقوق الملكية الفكرية البحثية الخاصة بها فائدة في إقامة شراكات وتوليد الإيرادات دون الحاجة إلى منتج معتمد من إدارة الغذاء والدواء، بالإضافة إلى تدفق السيولة النقدية حتى عام 2026.
وبما أن Cas12a يبدو أنه أصبح أكثر إثباتًا باعتباره أفضل طريقة في فئتها لتحرير الجينات المتعددة، فإن خبرة Editas وتركيز خط الأنابيب على هذا المتغير من CRISPR قد يكون رهانًا رابحًا على المدى الطويل.
(يمكنك قراءة المزيد عن شركات CRISPR في مقالتنا المقابلة "أفضل 5 شركات كريسبر للاستثمار فيها".)
أحدث أخبار وتطورات أسهم Editas (EDIT)
الدراسات المشار إليها:
1. نوري، ف.، علي باباي، ف.، فوروزان مهر، ب.، طهماسيبي، ح.، أوكسينيتش، ف.، وإسلامي، م. (2025). التقدم في تقنية كريسبر للعلاجات المضادة للفيروسات: تحرير الجينوم كعلاج محتمل للعدوى الفيروسية المزمنة. بحوث علم الأحياء الدقيقة، 16(5)، 104. https://doi.org/10.3390/microbiolres1605010