ביוטק
CRISPR מהדור הבא משפר את הדיוק בריפוי גנטי
Securities.io מקפיד על סטנדרטים מחמירים של עריכה ועשוי לקבל פיצוי מקישורים שנבדקו. איננו יועצי השקעות רשומים וזה אינו ייעוץ השקעות. אנא עיינו באתר שלנו גילוי נאות.

הפיכת עריכת גנים למדויקת יותר
עד לאחרונה, מודיפיקציות גנטיות היו גסות למדי, והכניסו רצף גנטי חדש באופן אקראי לאורגניזמים המטרה.
שיטת ההחדרה הייתה גם הרסנית מאוד. כתוצאה מכך, רק חיידקים וצמחים היו עוברים שינוי גנטי באופן שגרתי, וכל עריכה גנטית באורגניזמים כמו יונקים (כולל בני אדם) הייתה מורכבת, יקרה ואיטית.
זה השתנה חלקית עם טכנולוגיית CRISPR, אשר פתחה לפתע את הדרך לעריכת גנים מדויקת ומבוקרת, וכתוצאה מכך אושר הריפוי הגנטי הראשון למחלות גנטיות אנושיות בסוף 2023.
עם זאת, CRISPR עדיין אינו מושלם, ולעיתים מוביל לשינויים גנטיים לא רצויים.
ייתכן שזה השתנה עם תגלית פורצת דרך של שלושה חוקרים ב-MIT.
הם הכריזו על שיטה חדשה המאפשרת שיפור דרמטי באמינות עריכת גנים, וסוללת את הדרך ליצירת טיפולים חדשים.
הם פרסמו את תוצאותיהם בכתב העת המדעי היוקרתי Nature1, תחת הכותרת "עורכי פריים מהונדסים עם שגיאות גנומיות מינימליות".
מ-CRISPR רגיל לעריכת פריים
מאז אישור הטיפולים הראשונים המבוססים על CRISPR-Cas9, הרעיון של עריכה אמינה של הגנום של חולים כדי לרפא אותם כבר אינו מדע בדיוני. עם זאת, טכנולוגיית CRISPR לא תמיד משנה את הגן הממוקד כפי שהמדענים מתכוונים.
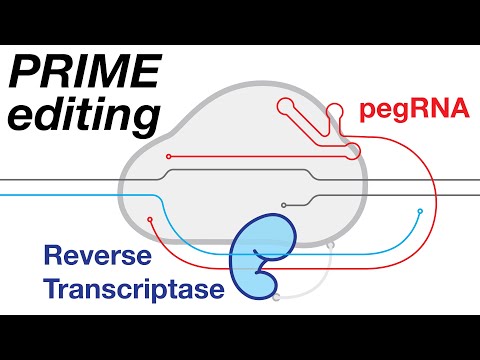
מערכת CRISPR מורכבת מאנזים בשם Cas9 שיכול לחתוך DNA דו-גדילי בנקודה מסוימת, יחד עם RNA מנחה שאומר ל-Cas9 היכן לחתוך.
חוקרים אימצו גישה זו כדי לחתוך רצפי גנים פגומים או להכניס חדשים, בהתאם לתבנית RNA.
מאז 2019, חוקרים ב-MIT פרסמו קונספט חדש בשם עריכה ראשונית, שהוא מדויק יותר מעריכת גנים רגילה של CRISPR-Cas9. כתוצאה מכך, יש לה פחות השפעות מחוץ למטרה ופחות סיכוי לגרום לבעיות בריאותיות נוספות לחולים, שלעתים קרובות כבר חלשים.
עריכה ראשונית משתמשת ב-Cas9 שעבר שינוי הממוזג עם אנזים רוורס טרנסקריפטאז, מה שמאפשר לו לבצע את כל השינויים האפשריים בבסיס הגנטי, כמו גם הוספות ומחיקות קטנות של רצפים גנטיים.
אז בטווח הארוך, עריכה ראשונית צפויה להפוך לגרסה משודרגת ואמינה יותר של עריכת גנים מבוססת CRISPR.

מקור: בנג'מין מקלאוד
לדוגמה, עורכים ראשיים שימשו בהצלחה בשנת 2025 לטיפול בחולה עם מחלת גרנולומטוטית כרונית (CGD), מחלה גנטית נדירה הפוגעת בתאי דם לבנים.
"בעיקרון, טכנולוגיה זו תוכל בסופו של דבר לשמש לטיפול במאות רבות של מחלות גנטיות על ידי תיקון מוטציות קטנות ישירות בתאים וברקמות."
אבל זה היה צריך שיפור קטן לפני שיהיה מוכן לשימוש בתאים ובגוף של אנשים.
כיצד עריכה ראשונית משפרת את דיוק החדרת ה-DNA
עריכה ראשונית חותכת רק אחד מהגדילים המשלימים של רצף ה-DNA של המטרה, ופותחת פתח שבו ניתן להכניס רצף חדש.
עם זאת, לאחר שהרצף החדש הועתק, עליו להתחרות עם גדיל ה-DNA הישן כדי להשתלב בגנום.
אם הגדיל הישן מתחרה בחדש, הכנף הנוספת של ה-DNA החדש שנוצרה תלויה בטעות עלולה להשתלב במקום אחר, ולגרום לשגיאות.
שגיאות כאלה עלולות בסופו של דבר לגרום לסרטן על ידי החדרת עצמן באופן אקראי לגנום, סיכון ברור שיש להפחיתו.
עם הגרסה העדכנית ביותר של עורכי הפריים, שיעור השגיאות הזה נע בין אחת לכל שבע עריכות לאחת לכל 121 עריכות עבור מצבי עריכה שונים, וזה עדיין גבוה מדי.
"הטכנולוגיות שיש לנו כיום טובות בהרבה מכלי ריפוי גנטי קודמים, אבל תמיד יש סיכוי לתוצאות לא מכוונות כאלה",
קפיצת מדרגה משמעותית באמינות עריכת פריים
בשנת 2023, חוקרי MIT גילו כי גרסאות מוטנטיות מסוימות של חלבון Cas9 המשמשות בעריכה ראשונית לפעמים נכנסות לבסיס אחד או שניים קדימה ברצף ה-DNA, במקום להיות תמיד באותו מקום.
זה הפך את גדילי ה-DNA הישנים לפחות יציבים, ולכן הם מתכלים, מה שמקל על שילוב הגדילים החדשים מבלי לגרום לשגיאות.
במחקר חדש זה משנת 2025, החוקרים זיהו מספר מוטציות Cas9 אשר מזהות מוטציות Cas9 שהורידו את שיעור השגיאה ל-1/20 מערכו המקורי.
כאשר שילבו את המוטציות הללו באופן מלאכותי בחלבון Cas9 אחד, הם הורידו את שיעור השגיאה ל-1/36 מהכמות המקורית.
"מאמר זה מתאר גישה חדשה לעריכת גנים שאינה מסבכת את מערכת ההעברה ואינה מוסיפה שלבים נוספים, אך מביאה לעריכה מדויקת הרבה יותר עם פחות מוטציות לא רצויות."
הם לא הסתפקו בכך, אלא גם השתמשו במערכת עריכה מעולה הכוללת חלבון קושר RNA שמייצב את קצוות תבנית ה-RNA בצורה יעילה יותר.
הגרסה הסופית של ערכת הכלים לעריכת גנים שלהם, שכונתה vPE, הכילה שיעור שגיאות של רק 1/60 מהמקור, או רק 101-543 עריכות, בהתאם למצבי העריכה שבהם נעשה שימוש.
החלק כדי לגלול →
| גרסת עורך ראשי | שיעור שגיאות משוער | שיפור לעומת מקורי |
|---|---|---|
| עורך ראשי מקורי | שגיאה אחת לכל 7–121 עריכות | Baseline |
| גרסאות Cas9 מוטנטיות | שיעור שגיאה מקורי של 1/20–1/36 | עד פי 36 יותר מדויק |
| vPE (מיוצב על ידי RNA) | שיעור שגיאה מקורי של 1/60 | עד פי 60 יותר מדויק |
השלבים הבאים
מכשול נוסף בעריכת גנים תמיד היה העברת חלבוני עריכת הגנים וה-DNA/RNA לתוך גרעין התאים הממוקדים, או מיקוד רק ברקמות ספציפיות בגוף.
אז זה יהיה המוקד הבא של החוקרים, במיוחד מכיוון שטכניקות עריכה מובילות מוגבלות עקב אספקה גרועה בהשוואה למערכות CRISPR-Cas9 "מסורתיות" קטנות ופשוטות יותר.
הם גם חושבים שלכלי זה יש פוטנציאל להאיץ את ההתקדמות בביוטכנולוגיה באופן כללי, לא רק עבור טיפולי עריכת גנים.
ראשית, הטכניקה והגילוי לפיהן שינוי של חלבון Cas9 יכול לשפר את אמינותו ניתנות לפריסה בכל טכנולוגיות עריכת גנים מבוססות CRISPR, לא רק על עריכה ראשונית.
שנית, הדבר יכול להוות דחיפה משמעותית לפרויקטים מחקריים אחרים המשתמשים בעריכת גנים וגנום ככלי מחקר. לדוגמה, מציאת תשובות לגבי התפתחות רקמות, התפתחות אוכלוסיות של תאי סרטן וכיצד תאים מגיבים לטיפול תרופתי.
"עורכי גנום נמצאים בשימוש נרחב במעבדות מחקר."
אז ההיבט הטיפולי הוא מרגש, אבל אנחנו ממש נרגשים לראות איך אנשים מתחילים לשלב את העורכים שלנו בתהליכי העבודה המחקריים שלהם."
לבסוף, ייתכן שלא כל המוטציות שנמצאו כמשפרות את אמינות Cas9 נמצאו במחקר זה. לכן, ניתוח ואופטימיזציה נוספים של מושג חדש זה עשויים להניב תוצאות טובות אף יותר בעתיד.
השקעה בעריכת גנים
Illumina
(ILMN )
בעוד -אומיקס אחר במולטיאומיקס (פרוטאומיקה, טרנסקריפטומיקה וכו') חשובים, כמעט כולם מתבטאים בצורה כזו או אחרת סביב הגנומיקה, "מדריך ההוראות" הליבה של כל תא חי.
והיצרן הגדול ביותר של מכונות ריצוף גנום הוא Illumina. החברה מתמקדת בקריאת רצפים גנטיים קצרים, המשמשים לגילוי סרטן. כיום יש לה יותר מ-22,000 מכונות ריצוף מותקנות ב-165 מדינות.
כמחצית מהחומרים המתכלים של מכונות הריצוף של אילומינה משמשים ביישומים קליניים, בעוד שהמחצית השנייה משמשת במעבדות מחקר ציבוריות ופרטיות. ביישומים קליניים, מחצית מהביקוש מגיע מאונקולוגיה.

מקור: Illumina
ככל שגנומיקה ומולטיומיקה הופכות למרכז תהליך גילוי תרופות, כמו גם אבחון סרטן, ציוד של אילומינה צפוי להיות מבוקש מאוד.
החברה צופה כי הביקוש ל-NGS (ריצוף הדור הבא) יגדל ב-18% CAGR עבור יישומים קליניים וב-6% CAGR עבור מחקר, מה שיגדיל את סך שוק הפתיחה (TAM) של המגזר מ-100 מיליארד דולר עבור יישומים קליניים ול-25 מיליארד דולר עבור מחקר עד 2033.

מקור: Illumina
לאילומינה הייתה היסטוריה מסובכת עם חברת הביופסיה הנוזלית Grail (GRAL -0.36%), שהייתה חברת ספין-אוף של אילומינה, שנרכשה מחדש מאוחר יותר, וכעת נאלצה לחזור לתחום הספין-אוף על ידי רשויות התחרות בארה"ב ובאיחוד האירופי.
לאחר פתרון הבעיה הזו, אילומינה עשויה לחדש את הצמיחה ארוכת הטווח ואת עליית מחירי המניה, במיוחד מכיוון שבסופו של דבר, בדיקות הביופסיה הנוזלית של גריל עדיין יסתמכו על רצפי בדיקות של אילומינה.
בינתיים, טיפולים גנטיים נוספים יגדילו גם את השימוש ברצפוצי המחקר של אילומינה הן במחקר והן בקליניקה.
(אפשר גם לקרוא ניתוח מפורט יותר של עסקיה של אילומינה, טכנולוגיותיה העתידיות וההיסטוריה שלה בדוח ההשקעות הייעודי.)
חדשות ופיתוח אחרונות של מניית אילומינה (ILMN)
מחקר שאליו התייחס
1. צ'אוהאן, סגן נשיא, שארפ, פנסילבניה ולנגר, ר. עורכי פריים מהונדסים עם שגיאות גנומיות מינימליות. טבע (2025). https://doi.org/10.1038/s41586-025-09537-3











