BioTech
Robots de ADN explicados: El futuro de la medicina y la informática

Adopción de robots está avanzando rápidamente, impulsado por la disminución de los costos, el aumento de la demanda y la integración de la inteligencia artificial (IA).
Según el Estadísticas del Campeonato Mundial de Robótica 2025 En el sector de los robots industriales, se instalaron 542,000 robots en 2024. Esto supuso la "segunda cifra anual más alta de instalaciones de robots industriales de la historia, solo un 2 % inferior al máximo histórico alcanzado hace dos años", declaró Takayuki Ito, presidente de la Federación Internacional de Robótica.
Además de en las fábricas, los robots también se están desplegando activamente en aeropuertos, campos agrícolas, oficinas, el ejército y el espacio exterior, a medida que evolucionan de máquinas rígidas y preprogramadas a sistemas inteligentes y adaptables.
Los robots ya no son meros brazos mecánicos; por el contrario, se están volviendo más inteligentes, más pequeños y mucho más versátiles gracias a los avances en la ciencia de los materiales, la miniaturización y la inteligencia artificial.
Esto ha dado lugar a una profunda transformación en la medicina, donde los robots quirúrgicos permiten realizar procedimientos mínimamente invasivos con una precisión nunca antes alcanzada. Mientras tanto, la microrrobótica y los sistemas bioingenieriles prometen terapias dirigidas que pueden reducir significativamente los efectos secundarios.
Incluso la idea de que existan máquinas operando dentro del cuerpo humano se está convirtiendo rápidamente en una realidad científica.
Entrando en la era de la robótica molecular
Una nueva frontera en robótica es una clase emergente de máquinas microscópicas Construido a partir de ADN y diseñado para funcionar dentro del cuerpo humano.
El concepto de nanotecnología del ADN fue introducido hace varias décadas por el profesor Nadrian Seeman, ampliamente reconocido como el padre fundador de este campo. Sin embargo, el progreso en este ámbito fue lento en sus inicios debido a los altos costos y la inmadurez de las tecnologías de síntesis de ADN.
Los avances en la síntesis química del ADN a principios del siglo XXI redujeron drásticamente los costes de producción y aceleraron el desarrollo de la nanotecnología del ADN.
Un avance importante se produjo hace dos décadas, cuando Paul Rothemund introdujo la técnica del origami de ADN, que permitió la creación de nanoestructuras mediante el autoensamblaje de ADN de abajo hacia arriba y que desde entonces se ha convertido en una de las estrategias más adoptadas para la construcción de robots de ADN.

Estos diminutos dispositivos están construidos con moléculas biológicas que pueden desplazarse por el cuerpo, interactuar con las células y realizar tareas muy específicas. Dado que estos sistemas están fabricados con el mismo material fundamental que recorre el cuerpo, a diferencia de los robots tradicionales, pueden funcionar sin problemas en entornos biológicos.
Un nuevo estudio publicado en la revista SmartBot1 pone de manifiesto lo mucho que ha avanzado este campo. Esto demuestra la evolución de las máquinas de ADN, desde las primeras ideas hasta sistemas más complejos, prácticos y capaces que algún día podrían administrar medicamentos directamente a las células enfermas o incluso identificar y neutralizar virus dentro del cuerpo.
Su potencial va mucho más allá, abarcando el análisis de moléculas individuales, la nanofabricación a nivel atómico e incluso la construcción de dispositivos informáticos y sistemas de almacenamiento de datos extremadamente pequeños.
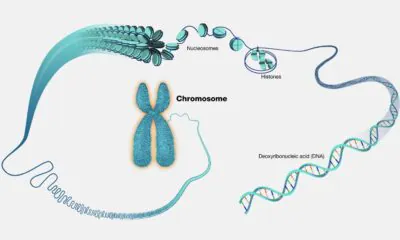
En su detallado análisis, investigadores de la Universidad de Pekín (PKU) explican cómo se está utilizando el ADN para crear máquinas funcionales. Aquí se utiliza el mismo ADN, ácido desoxirribonucleico, que contiene la información genética en casi todos los organismos vivos. Se trata de un material de construcción ideal y versátil para la creación de robots microscópicos con geometrías complejas, dimensiones definidas con precisión y capacidades multifuncionales.
Esto se debe a la facilidad de síntesis del ADN, su capacidad de autoensamblaje preciso, su estabilidad estructural y su programabilidad. Según el estudio, la molécula ofrece una ventaja particularmente singular en cuanto a "programabilidad mecánica". Si bien las cadenas simples (ssDNA) brindan flexibilidad, las secciones de doble cadena (dsDNA) añaden estructura a los diseños, y juntas proporcionan un conjunto claro de herramientas de diseño.
Debido a estas propiedades, junto con los avances en la nanotecnología estructural del ADN, los robots de ADN, a menudo denominados nanomáquinas de ADN y nanorobots, han evolucionado rápidamente.
Para crear estos diminutos robots, los científicos están combinando la robótica tradicional con técnicas de plegado de ADN, lo que permite el movimiento y la realización de tareas de forma fiable y con gran precisión.
Los robots de ADN aún se encuentran en sus primeras etapas y se enfrentan a importantes obstáculos. A pesar de estos desafíos, el campo avanza a medida que los científicos aprenden a diseñar estructuras de ADN capaces de doblarse, agarrar, plegarse y moverse a voluntad.
De este modo, el trabajo pone de relieve un futuro en el que estas máquinas biológicas programables podrán servir como herramientas de precisión para el diagnóstico, el tratamiento y la prevención de enfermedades, transformando potencialmente la medicina en su esencia.
«Los robots del futuro no estarán hechos solo de metal y plástico», señaló el equipo de investigación. «Serán biológicos, programables e inteligentes. Serán las herramientas que nos permitirán dominar finalmente el mundo molecular».
Superando el desafío del movimiento molecular
Para construir máquinas moleculares, los investigadores llevan mucho tiempo explorando el ADN, investigando cómo se puede modificar para convertirlo en máquinas funcionales.
Los diseños de los primeros dispositivos de ADN eran muy simples; podían abrirse y cerrarse o moverse a lo largo de una pista. Si bien eran simples, demostraron que el movimiento a nivel molecular era posible.
Ahora, los científicos están yendo más allá con enfoques de diseño creativos, que incluyen la incorporación de componentes flexibles, la construcción de uniones de ADN firmes para mayor estabilidad y el uso de métodos de plegado inspirados en el origami.
En el origami de ADN, largas hebras se pliegan para formar figuras complejas. Los investigadores utilizan cientos de hebras más pequeñas para guiar una sola y crear formas detalladas como cajas, jaulas y engranajes. Si bien algunos diseños pueden tener miles de componentes, otros funcionan como pequeños interruptores, mecanismos de movimiento o pinzas.
Así pues, los investigadores están aplicando principios de la robótica tradicional a gran escala a la nanoescala, lo que permite que los sistemas basados en ADN realicen tareas repetibles y controladas.
Pero convertir el ADN en máquinas requiere no solo estructura, sino también movimiento, y el tamaño extremadamente pequeño de estos robots de ADN supone un gran desafío para guiar su movimiento en el entorno molecular caótico y en constante cambio.
| Área clave | Situación actual | Enfoque del sistema | Por qué es Importante |
|---|---|---|---|
| Material del núcleo | Los robots convencionales dependen de metales, chips y motores. | Utilizar el ADN como material de construcción programable. | Permite que las máquinas funcionen dentro de entornos biológicos. |
| Diseño estructural | Los sistemas mecánicos se ensamblan a partir de componentes rígidos. | Dobla las hebras de ADN formando cajas, uniones y jaulas. | Permite construir arquitecturas precisas a nanoescala. |
| Control de Movimiento | El movimiento molecular aleatorio altera el comportamiento de las máquinas a nanoescala. | Dirigir el movimiento mediante reacciones o señales de ADN. | Hace posible una acción molecular predecible. |
| Uso Médico | Muchas terapias siguen afectando también a los tejidos sanos. | Administrar los fármacos únicamente en las células afectadas por la enfermedad. | Podría mejorar la precisión al tiempo que reduce los efectos secundarios. |
| Escala de fabricación | La producción de máquinas de ADN idénticas sigue siendo difícil y costosa. | Desarrollar métodos de biofabricación fiables y de alto rendimiento. | Imprescindible para su aplicación en el mundo real, más allá de los laboratorios. |
| Desarrollo futuro | Las herramientas de diseño y las simulaciones aún están poco desarrolladas en la actualidad. | Utilizar la IA para optimizar el diseño y el comportamiento. | Podría acelerar el progreso en medicina e informática. |
Para controlar el movimiento de estas máquinas, los científicos han desarrollado sistemas que les permiten comportarse de forma predecible. Esto incluye reacciones bioquímicas y señales físicas como calor, luz, campos magnéticos y campos eléctricos.
En lo que respecta al control bioquímico, el método que utilizan los investigadores es el desplazamiento de hebras de ADN, un proceso que permite programar con precisión el movimiento mediante secuencias de ADN que actúan como "combustible" y "estructura". En este proceso, una hebra desplaza a otra, funcionando como un interruptor molecular que puede desencadenar un movimiento específico.
Sin embargo, cada método conlleva ventajas e inconvenientes, lo que obliga a los científicos a encontrar un equilibrio entre precisión y velocidad.
Por ejemplo, el control químico ofrece precisión y versatilidad, pero genera moléculas de desecho y requiere un extenso proceso de selección experimental. Por otro lado, las señales físicas externas actúan con rapidez, pero afectan a los sistemas circundantes. Si bien mueven estructuras completas, tienen dificultades para permitir un control independiente a nivel articular.
Mediante la combinación de estas estrategias, los científicos proporcionan un conjunto de herramientas para ajustar con gran precisión el comportamiento de las máquinas de ADN. En lo que respecta a la aplicación de estas máquinas microscópicas, el estudio señala que van mucho más allá del laboratorio.
Para empezar, los robots de ADN pueden ser de gran ayuda en la medicina de precisión, donde pueden actuar como "nanocirujanos" dentro del cuerpo, identificando células enfermas y administrando terapias a esas células.
En un ejemplo con un robot de ADN, se logró capturar el SARS-CoV-2 de la saliva en media hora utilizando cuatro dedos flexibles, y su rendimiento fue comparable al de las pruebas de laboratorio convencionales. En otro caso, el robot transportó un fármaco coagulante a los vasos sanguíneos de tumores en ratones y lo administró solo al alcanzar el objetivo, demostrando su potencial como sistema autónomo de administración de fármacos.
Los robots de ADN también pueden servir como plantillas programables para organizar materiales, lo que permite crear dispositivos ópticos moleculares, dispositivos informáticos y sistemas de almacenamiento de datos ultradensos más eficientes que la tecnología actual.
Las guías de ADN, las nanopartículas y las fuentes de luz ya se han dispuesto en patrones ordenados. En experimentos relacionados, los investigadores también han impreso marcas químicas en ADN sintético y codificado imágenes sin escribir cada base de nuevo. Por lo tanto, las posibilidades que ofrecen estas máquinas de ADN son simplemente extraordinarias.
Pero, por supuesto, todo esto aún se encuentra en fases experimentales iniciales. Dado que todavía están lejos de tener aplicaciones prácticas en el mundo real, estos robots de ADN deben entenderse mejor como una prueba de concepto. De hecho, la puesta en marcha de estas máquinas plantea varios desafíos. La escala es uno de ellos.
Cuando pasamos de sistemas a gran escala a sistemas a nanoescala (aproximadamente 100 nm, entre 1/500 y 1/1000 del grosor de un cabello humano), el control preciso de estas máquinas se vuelve difícil debido al movimiento browniano, que es el pequeño movimiento aleatorio de las nanopartículas, y a las fluctuaciones térmicas. El estudio señaló:
“Si bien la robótica macroscópica ofrece valiosos marcos conceptuales y analíticos, trasladar sus principios a la escala molecular y nanométrica exige una profunda redefinición del diseño mecánico y del control del movimiento bajo restricciones estocásticas, termodinámicas y bioquímicas.”
Por eso, muchos de los diseños de robots basados en ADN existentes son sencillos y funcionan de forma aislada. Su utilidad en entornos complejos del mundo real también es limitada.
Pero los sistemas futuros deben ser escalables, reconfigurables e integrados funcionalmente, lo que depende de la adopción de una modularidad avanzada y de la traducción de los principios mecánicos a macroescala al nivel molecular.
Luego está el problema de las lagunas de conocimiento. Incluso hoy en día, los investigadores carecen de información detallada y comprensión de las propiedades mecánicas de las estructuras del ADN. Las herramientas de modelado y simulación computacional para predecir cómo se comportan estas estructuras a escalas microscópicas aún no están completamente desarrolladas.
La fabricación supone otro obstáculo. Producir máquinas de ADN idénticas a gran escala es necesario para sus aplicaciones prácticas, pero requiere métodos rentables, de alto rendimiento y fiables que aún son difíciles de conseguir.
Según el estudio, superar todas estas barreras requiere la colaboración de diversas disciplinas: ingeniería mecánica, informática, medicina, química y biología.
Más concretamente, los científicos proponen soluciones como el avance de los métodos de biofabricación, la creación de "bibliotecas de componentes" de ADN estandarizadas y el uso de la IA para mejorar el diseño y la simulación.
Según el estudio, el aprendizaje profundo y los modelos de lógica difusa (LLM) ofrecen «oportunidades transformadoras para el avance del diseño y el análisis de máquinas de ADN», así como para la simulación y el análisis dinámico. Esta tecnología permite descubrir patrones estructurales a partir de grandes conjuntos de datos, predecir rutas de plegamiento, optimizar configuraciones de secuencias y automatizar la evaluación del diseño, acelerando significativamente el ciclo de innovación.
Los avances en estas áreas ayudarán a ampliar la escala de los robots de ADN y a integrarlos en aplicaciones prácticas en la ciencia, la atención médica, la fabricación y otros ámbitos.
Invertir en tecnología de robótica de ADN
En el mundo de la robótica médica, Illumina, Inc. (ILMN ) Destaca por su sólida experiencia en tecnologías de ADN y su fuerte posicionamiento en la medicina basada en la genómica. Si bien la empresa no fabrica robots de ADN, es un importante impulsor de todo el ecosistema que hace posibles estas innovaciones.
Líder mundial en secuenciación de ADN, la compañía proporciona las herramientas fundamentales que permiten la investigación en sistemas basados en ADN, incluyendo la nanotecnología de ADN y la robótica. Asimismo, está profundamente involucrada en la transición hacia la medicina personalizada y molecular.
Los productos de la compañía se utilizan en investigación y clínica, así como en oncología, ciencias biológicas, salud reproductiva, agricultura y otros sectores. Entre sus clientes se incluyen instituciones académicas, centros de investigación genómica, hospitales, laboratorios gubernamentales, laboratorios comerciales de diagnóstico molecular, empresas de biotecnología, farmacéuticas y de genómica de consumo.
El objetivo de Illumina es mejorar la salud humana liberando el poder del genoma. El mes pasado, Illumina anunció una colaboración estratégica con Veritas Genetics para incorporar la secuenciación del genoma completo a la atención médica cotidiana a través de los sistemas de seguros.
Esta colaboración impulsa un ecosistema de datos integrado para fomentar la investigación, el descubrimiento de fármacos y la optimización de ensayos clínicos. Y lo que es aún más importante, marca un cambio: de tratar enfermedades a predecirlas y prevenirlas mediante datos genéticos.
«La genómica está cada vez más presente en la atención médica, desde el diagnóstico de enfermedades hasta su prevención», afirmó Rami Mehio, director general de BioInsight en Illumina. «Al combinar la infraestructura de secuenciación e informática de Illumina con los informes listos para el paciente de Veritas, esta colaboración representa un importante avance para que la genómica preventiva sea práctica, accesible e integrada en la atención médica diaria».
Un par de meses antes, Illumina presentó el Atlas de Mil Millones de Células, el conjunto de datos de perturbación genética a nivel genómico más grande del mundo, que podría hacer que los robots de ADN fueran prácticos y programables.
Este enorme conjunto de datos describe cómo miles de millones de células responden a los cambios genéticos, y se ha creado utilizando CRISPR y secuenciación. La primera fase del programa de la compañía para construir un atlas de 5 mil millones de células en tres años, que lo convertirá en "el mapa más completo de la biología de las enfermedades humanas hasta la fecha", está diseñada para entrenar modelos de IA y acelerar el descubrimiento de fármacos en colaboración con Merck, AstraZeneca y Eli Lilly and Company.
«Creemos que el atlas celular es un avance clave que nos permitirá escalar significativamente la IA para el descubrimiento de fármacos», declaró Jacob Thaysen, director ejecutivo de Illumina. «Estamos creando un recurso sin precedentes para entrenar a la próxima generación de modelos de IA para la medicina de precisión y la identificación de dianas farmacológicas, lo que en última instancia ayudará a trazar un mapa de las vías biológicas que subyacen a algunas de las enfermedades más devastadoras del mundo».
(ILMN )
En medio de estos avances, las acciones de Illumina, con una capitalización de mercado de 19.5 millones de dólares, cotizan a 127.74 dólares, un 74% más que el año anterior. Su beneficio por acción (últimos doce meses) es de 5.48 dólares y su ratio precio/beneficio (últimos doce meses) es de 23.32.
En cuanto a la solidez financiera de Illumina, en el cuarto trimestre de 2025, la compañía reportó ingresos de $1.16 mil millones, un aumento del 5% con respecto al cuarto trimestre de 2024. Su margen operativo GAAP fue del 17.4%, y su margen operativo no GAAP fue del 23.7%, mientras que la ganancia por acción diluida GAAP fue de $2.16 y la ganancia por acción diluida no GAAP fue de $1.35.
Durante este período, los gastos de capital ascendieron a 54 millones de dólares, mientras que el flujo de caja de las operaciones fue de 321 millones de dólares. Al cierre del ejercicio, la empresa contaba con 1.63 millones de dólares en efectivo, equivalentes de efectivo e inversiones a corto plazo.
Durante el ejercicio fiscal completo de 2025, Illumina registró unos ingresos de 4.34 millones de dólares. Por otro lado, su margen operativo según los PCGA fue del 18.6%, su margen operativo no PCGA fue del 23.1%, su beneficio por acción diluido según los PCGA fue de 5.45 dólares y su beneficio por acción diluido no PCGA fue de 4.84 dólares.
El año pasado, los gastos de capital ascendieron a 148 millones de dólares, mientras que el flujo de caja de las operaciones fue de 1.1 millones de dólares y el flujo de caja libre fue de 931 millones de dólares.
Al hablar del "sólido cierre de 2025", Thaysen afirmó que esto marca "un regreso al crecimiento a través de una ejecución disciplinada de nuestra estrategia", con un impulso generado en la segunda mitad del año pasado, especialmente con la creciente adopción de pruebas basadas en NGS en los mercados clínicos.
Cabe destacar que Illumina logró avances en China, donde se levantó la prohibición de exportación de sus secuenciadores. Sin embargo, sigue figurando en la Lista de Entidades No Confiables (UEL, por sus siglas en inglés), lo que exige autorizaciones para la compra de instrumentos.
Para el presente año, Illumina prevé un aumento de ingresos de entre el 4 % y el 6 %, alcanzando entre 4.5 y 4.6 millones de dólares. Este crecimiento incluye un beneficio de entre el 1.5 % y el 2 % derivado de la reciente adquisición de SomaLogic, que amplía la cartera de soluciones multiómicas de la compañía y fortalece su posición en el campo de la proteómica basada en secuenciación de nueva generación (NGS).
Últimas noticias y novedades sobre las acciones de Illumina, Inc. (ILMN)
Conclusión
Los robots han redefinido las capacidades de las máquinas. Han mejorado la productividad, la seguridad y la investigación en diversos ámbitos. Desde la automatización industrial hasta la exploración planetaria, la continua evolución de los robots pone de manifiesto una tendencia más amplia hacia la integración cada vez más profunda de sistemas más capaces en nuestras vidas.
En medicina, la aparición de robots biológicamente compatibles, como los sistemas basados en ADN, está permitiendo una precisión sin precedentes en la administración de fármacos y la focalización de virus.
Y lo que es más importante, estos sistemas prometen no solo tratamientos más precisos y mejores resultados para los pacientes, sino también una nueva forma de estudiar procesos a nivel molecular y de construir dispositivos más pequeños y potentes mediante el ensamblaje guiado por ADN.
Si bien es necesario abordar importantes desafíos en cuanto a escalabilidad, estabilidad y seguridad a largo plazo antes de que estas tecnologías puedan pasar de la investigación de laboratorio a la práctica clínica, los beneficios potenciales son considerables. Y a medida que la robótica continúa reduciendo su tamaño y ampliando sus capacidades, puede ofrecer un futuro en el que la medicina se ejecute de forma inteligente desde dentro.
Haz clic aquí para saber si la IA puede reescribir nuestro ADN.
Referencias
1. Xu, N., Zhang, X., Liu, Y., Wang, C., Li, J., Chen, Z., Zhao, H., Sun, K., Zhou, Q., Yang, F., Wu, T., Guo, S., Li, Y., Huang, J., Deng, D. & Bao, X. Diseñador de máquinas basadas en ADN. SmartBot (2026). https://doi.org/10.1002/smb2.70029